
Читайте также:
|
а) с внутренними индикаторами
Точную навеску препарата растворяют в смеси воды и хлороводородной кислоты, добавляют бромид калия (катализатор) и при постоянном перемешивании титруют 0,1н р-ром нитрита натрия при 18-20°С, иногда при 10°С. В качестве внутренних индикаторов используют тропеолин 00 переход окраски от красной к желтой, тропеолин 00 в смеси с метиленовым синим, титруют от красно-фиолетового до голубого окрашивания, с нейтральным красным - от малиновой окраски до синей.
| 0,1N |
| NH2 |
| SO2 - NH2 |
| + NaNO2 + 2 HCl |
| - NaCl - H2O |
| SO2 - NH2 |
| N+ N Cl |
Э=Мr.
 ,
, 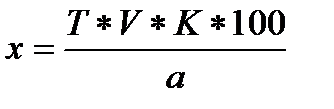
б) с внешним индикатором
Внешний индикатор - йодкрахмальная бумага: фильтровальная бумага, пропитанная раствором иодида калия и крахмала. Титрование с йодкрахмальной бумагой ведут до тех пор, пока капля титруемого р-ра, взятая через 1 минуту после прибавления р-ра нитрита натрия, будет немедленно вызывать синее окрашивание на бумаге.
| + NaCl + H2O |
| Cl - N+ N |
| + NaNO2 + 2 HCl |
| 0,1N |
| NH2 |
| SO2 - NH2 |
| SO2 - NH2 |
NaNO2 + 2KJ + 4HCl → J2 + 2NO + 2KCl + 2NaCl + 2H2O
ВОПРОСЫ ДЛЯ САМОКОНТРОЛЯ:
1. Какая реакция лежит в основе нитритометрии?
2. Как устанавливается титр раствора натрий нитрита?
3. Чему равен титр, молярность, поправочный коэффициент раствора NaNO2, если на титрование 0,1863 г сульфаниловой кислоты его израсходовано 11,6 мл?
4. Какие индикаторы применяют при нитритометрическом титровании?
Дата добавления: 2014-11-24; просмотров: 75 | Поможем написать вашу работу | Нарушение авторских прав |