
Читайте также:
|
6 м3 кислорода с начальной температурой t1= 60ºС и абсолютном давлении Р1= 0,4 МПа нагревается при постоянном давлении до температуры Т2 = 400ºС. Определить начальный и конечный объём газа и изменение энтропии (dS).
Решение:
V1 = 6 м3;
T1 = 60 ºС = 60+273,15 = 333,15 К;
T2 = 400 ºС = 400+273,15 = 673,15 К;
Р1= 0,4 МПа =0,4*106 Па = 400 000 Па;
R = 8,314 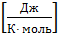 -газовая постоянная;
-газовая постоянная;
µ = 32*10-3 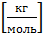 -молярная масса кислорода.
-молярная масса кислорода.
Воспользуемся уравнением Менделеева – Клайперона:
Для начального состояния уравнение имеет вид: 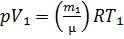
Для конечного состояния уравнение имеет вид: 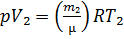 т.к. при постоянном давлении (изобарный процессе) Р = const выразим конечный объём:
т.к. при постоянном давлении (изобарный процессе) Р = const выразим конечный объём:
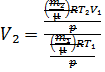 =
=  =
= 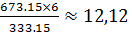 м3, или согласно закону Гей-Люссака, при изобарном процессе в идеальном газе:
м3, или согласно закону Гей-Люссака, при изобарном процессе в идеальном газе: 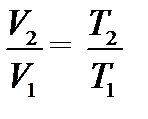 =>
=> 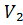 =
=  =
= 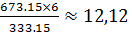 м3 .
м3 .
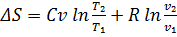 = (
= (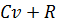 )
)  =
= 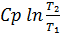 =
= 
Молярная теплоемкость газа при постоянном давлении Ср находится по формуле: Ср = ((i+2)/2)×R., где i - число степеней свободы молекулы газа. Так как О2 газ двухатомный, то его число степеней свободы i=12, => Ср=((12+2)/2) ×R. Ср =(14/2) ×8,314=58,198 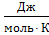
ΔS=  = 58,198 ln
= 58,198 ln  = 40,935
= 40,935 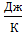
Ответ: V1=6 м3; V2=12,12м3; ΔS= 40,935 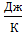 .
.
Дата добавления: 2015-04-11; просмотров: 19 | Поможем написать вашу работу | Нарушение авторских прав |