
Читайте также:
|
Константа диссоциации — вид константы равновесия, которая характеризует склонность объекта диссоциировать (разделяться) обратимым образом на частицы, как например когда комплекс распадается на составляющие молекулы, или когда соль диссоциирует в водном растворе на ионы. Константа диссоциации обычно обозначается Kd и обратна константе ассоциации. В случае с солями, константу диссоциации иногда называют константой ионизации.
В общей реакции

где комплекс 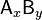 разбивается на x единиц A и y единиц B, константа диссоциации определяется так:
разбивается на x единиц A и y единиц B, константа диссоциации определяется так:

Связь константы диссоциации и степени диссоциации:
Исходя из определения степени диссоциации, для электролита КА в реакции диссоциации [A−] = [K+] = α·c, [KA] = c — α·c = c·(1 — α), где α — степени диссоциации электролита.
Тогда:
 , ,
| (2) |
Это выражение называют законом разбавления Оствальда. При очень малых α (α<<1) K=cα² и
 ,
,
таким образом, при увеличении концентрации электролита степень диссоциации уменьшается, при уменьшении — возрастает.
Закон разбавления Оствальда — соотношение, выражающее зависимость эквивалентной электропроводности разбавленного раствора бинарногослабого электролита от концентрации раствора:

Здесь 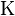 — константа диссоциации электролита,
— константа диссоциации электролита,  — концентрация,
— концентрация,  и
и  — значения эквивалентной электропроводности при концентрации
— значения эквивалентной электропроводности при концентрации  и при бесконечном разбавлении соответственно. Соотношение является следствием закона действующих масс и равенства
и при бесконечном разбавлении соответственно. Соотношение является следствием закона действующих масс и равенства

где  — степень диссоциации.
— степень диссоциации.
Дата добавления: 2015-02-16; просмотров: 210 | Поможем написать вашу работу | Нарушение авторских прав |