
Читайте также:
|
Содержание
1. Введение……………………………………………………………..3 стр.
2. Структура лактатдегидрогеназы…………………………………...4 стр.
3. Характеристика изоферментов ……………………………………5-6 стр.
4. Клинико-диагностическое значение……………………………….7-9 стр.
5. Список использованной литературы………………………………10 стр.
Введение
Лактатдегидрогена́за (ЛДГ, лактат, НАД+ оксидоредуктаза, дегидрогеназа молочной кислоты) - фермент углеводного обмена, катализирует важнейшую реакцию гликолиза — взаимопревращение пировиноградной и молочной кислот, т. е. реакцию, завершающую внутренний окислительно-восстановительный цикл гликолиза. Относится к ферментам класса оксидоредуктаз, подклассу оксидоредуктаз, действующих на группу СН—ОН субстрата, и подподклассу оксидоредуктаз, акцептором электронов для которых служат НАД или НАДФ.
Впервые лактатдегидрогеназа получена из отмытой мышцы Маергофом в 1909 году, а в 1940 году Штрауб получил её в кристаллическом виде.
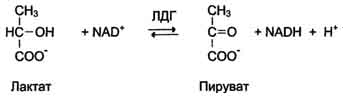
Фермент лактатдегидрогеназа (ЛДГ) катализирует обратимую реакцию окисления лактата (молочной кислоты) до пирувата (пировиноградной кислоты).
Структура лактатдегидрогеназы
Лактатдегидрогеназа - олигомерный белок, состоящий из 4 субъединиц 2 типов: М (от англ, muscle - мышца) и Н (от англ, heart - сердце).

Активный центр в субъединице ЛДГ. Пептидный остов белка изображен в виде ленты (светло-голубой), дополнительно представлены молекулы: субстрата — лактата (красного цвета), кофермента НАД+ (желтого цвета) и три боковые цепи аминокислот (зеленого цвета), которые участвуют непосредственно в катализе. Кроме того, выделена пептидная петля (малинового цвета), образованная аминокислотными остатками 98-111. В отсутствие субстрата и кофермента эта структура раскрыта, что обеспечивает свободный доступ к субстрат-связывающему участку (не показано).
Дата добавления: 2015-09-11; просмотров: 187 | Поможем написать вашу работу | Нарушение авторских прав |
| <== предыдущая лекция | | | следующая лекция ==> |
| Константин Матаков | | | Характеристика изоферментов |