
Читайте также:
|
В норме уровень глюкозы в плазме крови колеблется в пределах 3,3-5,5 мМоль/л – нормогликемия. Снижение ниже 3,3 мМоль/л – гипогликемия. Повышение выше 5,5 мМоль/л - гипергликемия. Снижение менее 2,7 мМоль/л - гипогликемическая кома. Увеличение более 8,8 мМоль/л – глюкозурия. Увеличение более 22 мМоль/л - гипергликемическая кома.
Инсулин - полипептидный гормон, состоящий из 2-х полипептидных цепей, обозначаемых как А- и В-цепи, соединенные двумя дисульфидными мостиками. Полная молекула содержит 51 аминокислоту с молекулярной массой 5800.
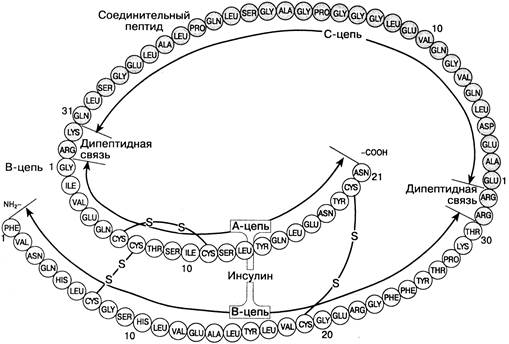
Рис. 14.8. Молекулы проинсулина и инсулина. Показаны последовательность аминокислот в молекуле проинсулииа, А- и В-цепи молекулы активного инсулина. Расщепление дипептидных связей ведет к образованию молекулы инсулина и неактивного С-пептида [по В.М. Кэттайл, Р.А. Арки, 2001].
Инсулин синтезируется бета-клетками в виде одноцепочечного предшественника – проинсулина (путем отщепления С-пептида), а тот, в свою очередь, из препроинсулина.
К стимуляторам синтеза и секреции инсулина относятся: глюкоза, манноза, лейцин, СТГ, глюкагон, глутаминовая кислота, секретин. Адреналин ингибирует синтез инсулина.

Рис. 14.9. Строение островкового аппарата поджелудочной железы.
В нормальных островках бетта-клетки составляют 60%, альфа-клетки - 25% (глюкагон) и дельта-клетки - 10% (соматостатин). Островок Лангерганса представляет собой маленький орган, все клетки которого координированно отвечают на стимулы извне и собственные паракринные влияния.
Главная функция инсулина - регуляция метаболизма белков, жиров, углеводов. Это анаболический гормон. Суммарно инсулин снижает уровень глюкозы в крови.
Его эффекты на мышцы, печень и жировую ткань:
стимуляция захвата клетками глюкозы, аминокислот, жирных кислот;
усиление синтеза гликогена (гликогеногенез в печени и мышцах);
усиление синтеза жиров - липогенез (ожирение при 2 типе СД), есть сведения, что тормозит липазу, но при 2 типе СД ожирение по андроидному типу (жир легко запасается и легко расщепляется), т.к. активируется липогенез и не тормозится липолиз;
усиление синтеза белков (протеиногенез);
стимуляция гликолиза;
торможение глюконеогенеза и распада гликогена (гликогенолиза), белков и триглицеридов.
50% инсулина распадается в печени под действием инсулиназы, поэтому при патологии печени развивается гиперинсулинемия.
Контринсулярные гормоны (увеличивают уровень глюкозы в крови);
Глюкагон (a-клеткиостровков Лангерганса поджелудочной железы):
ускоряет гликогенолиз и глюконеогенез в печени;
тормозит синтез белка и ускоряет протеолиз.
Глюкокортикостероиды (глюкокортикоиды) и АКТГ:
ускоряют глюконеогенез;
активируют гликогенолиз.
Адреналин:
активирует гликогенолиз,
активирует липолиз (ЖК - антагонисты инсулина)
СТГ:
активирует инсулиназу,
конкурирует с инсулином за рецепторы.
Соматостатин:
угнетает синтез инсулина и гликогена.
Гипогликемия – снижение концентрации глюкозы в плазме ниже нижней границы нормы.
Гипогликемия представляет собой снижение уровня глюкозы плазмы до таких значений, когда появляются клинические симптомы, исчезающие после нормализации снижения глюкозы.
Скорость развития гипогликемии зависит от пола больного, быстроты снижения уровня глюкозы, исходного содержания глюкозы.
В среднем принято считать, что гипогликемия развивается при снижении уровня глюкозы до 2,5-3,0 ммоль/л.
Классификация, основанная на характеристике условий, в которых развивает гипогликемия. С этих позиций можно выделить 3 основные виды гипогликемий:
I - гипогликемия натощак:
а) инсулинпродуцирующая опухоль бетта-клеток;
б) гипогликемия поврежденных с кетозом.
II - гипогликемия после еды:
а) спонтанная реактивная гипогликемия;
б) ранние стадии сахарного диабета.
III - индуцированная гипогликемия:
а) алкогольная гипогликемия;
б) передозировка инсулина.
Гипогликемия натощак характеризуется неэффективностью поддержания нормального уровня глюкозы в условиях воздержания от пищи.
В состоянии натощак глюкоза в организме человека потребляется почти исключительно мозгом. Небольшие количества ее потребляются также форменными элементами крови. Совершенно иная ситуация складывается в инсулинзависимых тканях, таких, как мышцы и жировая ткань, которые практических не потребляют глюкозу при голодании, длящемся 12 ч и более. Если голодание продолжается более 12-14 часов, то включаются дополнительные механизмы поддержания нормогликемии. Мозг утилизирует глюкозу со скоровстью 125 г/сут, поэтому запасов гликогена в печени явно недостаточно. На помощь приходит глюконеогенез и липолиз с последующим окислением жирных кислот и прогрессивным повышением в плазме уровня кетоновых тел (бета-оксимасляная кислота, ацетон и ацетоуксусная кислота). При более длительном голодании (дни и недели) в ход идут запасы белка, что неминуемо приводит к смерти (если вовремя не остановиться).
Таким образом, поддержание нормогликемии в состоянии натощак зависит от 3-х основных факторов:
гормональной среды, характеризующейся исходным или сниженным уровнем инсулина и исходным или повышенным уровнем глюкагона, СТГ и кортизола;
печени, в которой не нарушены процессы гликогенолиза и глюконеогенеза;
субстратов процессов глюконеогенеза.
Следовательно, гипогликемию натощак можно подразделить на эндокринную, печеночную и субстратную.
Итак, гипогликемия натощак подразделяется:
1. Эндокринная
а) Избыток инсулина или инсулиноподобных факторов:
островковоклеточные опухоли, продуцирующие инсулин;
внепанкреатические опухоли, вызывающие гипогликемию.
б) Дефицит СТГ:
гипопитуитаризм;
изолированный дефицит СТГ.
в) Дефицит кортизола:
гипопитуитаризм;
изолированный дефицит АКТГ;
Аддисонова болезнь.
2. Печеночная
а) болезни накопления гликогена;
б) дефицит ферментов глюконеогенеза;
в) острый некроз печени:
отравления;
вирусный гепатит.
г) застойная сердечная недостаточность.
3. Субстратная
а) гипогликемия беременных;
б) гипогликемия новорожденных с кетозом;
в) уремия;
г) алиментарная недостаточность.
4. Прочие причины
а) аутоиммунная инсулиновая гипогликемия.
Островковоклеточные опухоли поджелудочной железы вызывают гипогликемию за счет гиперпродукции инсулина. Состоит опухоль из гроздьев типичных бета-клеток. Патогенез гипогликемии у таких больных сводится либо к абсолютному повышению уровня инсулина в плазме натощак или во время физической работы, либо к отсутствию снижения уровня инсулина, которое в таких условиях происходит в норме.
Гипогликемия при дефиците гормонов обусловлена снижением или отсутствием их контринсулярного эффекта.
Гипогликемия при заболеваниях печени была частично нами уже рассмотрена (гликогенозы). Следует отметить, что это состояние встречается, и нередко, при вирусных гепатитах и тяжелых токсических поражениях печени.
Помимо снижения уровня инсулина, присутствия регуляторных гормонов и сохранности глюконеогенеза в печени, продукция глюкоза натощак требует и присутствия субстратов-предшественников, особенно аланина. У здоровых лиц скорость высвобождения аланина из мышц определяет скорость глюконеогенеза при голодании.
Гипогликемия после еды, или реактивная гипогликемия - это состояние можно определить как уменьшение содержания глюкозы в плазме в период перехода от состояния сытости к состоянию голода, достаточное для появления субъективных жалоб. Предполагают, что гипогликемия после еды может быть обусловлена либо отсутствием адекватного снижения утилизации глюкозы по мере уменьшения уровня глюкозы в плазме, либо неадекватностью поглощения глюкозы печенью и периферическими тканями.
В этой группе выделяют
идиопатическую (функциональную) гипогликемию,
алиментарную гипогликемию,
гипогликемию на ранних стадиях сахарного диабета.
Идиопатическая (функциональная) гипогликемия встречается чаще у женщин 25-35 лет, больные внешне не отличаются от здоровых. Жалобы достаточно неспецифичны - тошнота, слабость, сердцебиение. Симптомы эти могут существовать годами, не прогрессируя.
Алиментарная гипогликемия наблюдается иногда у больных с операциями на ЖКТ. Гипогликемия выражена больше, чем у больных с идиопатической гипогликемией. Считают, что гипогликемия у них обусловлена кишечными, а не панкреатическими дефектами.
Давно известно, что гипогликемия после еды может быть проявлением инсулиннезависимого СД (II типа, диабета взрослых). У таких больных натощак уровень глюкозы находится в пределах нормы, но рано повышается вследствие недостаточной секреции инсулина и отмечается поздняя гиперинсулинемия.
Из других причин гипогликемию после еды наблюдали при ожирении, почечной глюкозурии и различных гормондефицитных состояниях.
Индуцированные гипогликемии возникают при:
передозировке инсулина и других ССП;
приеме алкоголя;
врожденных дефектах метаболизма.
Алкогольная гипогликемия распространена среди пьющих, но мало или совсем не закусывающих лиц. Синдром развивается спустя 6-24 часа после алкогольного эксцесса и поэтому запах алкоголя может не ощущаться.
Механизм развития алкогольной гипогликемии, вероятно, заключается в уменьшении продуцирования глюкозы печени из-за угнетения алкоголем глюконеогенеза (снижение использования лактата и аланина).
Клинические проявления гипогликемии обусловлены двумя факторами: 1) снижением уровня глюкозы в головном мозге (нейрогликопения); 2) стимуляцией симпатоадреналовой системы.
Нейрогликопения проявляется головной болью, утомляемостью, помрачением сознания, галлюцинациями, судорогами и комой.
Симптомы адренергической стимуляции включают сердцебиение, возбуждение, потливость, дрожь и чувство голода. Они появляются раньше, чем все прочие, предупреждая о надвигающейся коме. Приступ можно оборвать, приняв глюкозу или углеводсодержащую пищу.
Лечение гипогликемии заключается в замедленном введении 50-70 мл 40% раствора глюкозы, можно повторно.
§ Этиология гипергликемических состояний. Диабеты. Патогенез сахарного диабета 1 и 2 типа. Понятие о почечном сахарном диабете.
Дата добавления: 2015-09-11; просмотров: 76 | Поможем написать вашу работу | Нарушение авторских прав |
| <== предыдущая лекция | | | следующая лекция ==> |
| Патология углеводного обмена. Сахарные диабеты. | | | Классификация диабетов |