
Читайте также:
|
Признаки химической реакции
1. Изменение окраски:
2. Выделение или поглощение теплоты:
3. Образования осадка:
4.. Выделение газа:
В настоящее время известно более 10 миллионов веществ, которые можно разделить (наряду с другими классификациями) на простые и сложные.
1) простые вещества – это вещества, состоящие из атомов одного и того же химического элемента (водород Н2, кислород О2, железо Fe)
2) сложные вещества или химические соединения, – это вещества, состоящие из атомов разных химических элементов.(вода Н2О, CaCO3)
Один и тот же элемент может образовывать разные простые вещества – это явление называется аллотропией.
Различные простые вещества, состоящие из атомов одного элемента, называются аллотропнымит модификациями. Явление аллотропии может быть вызвано двумя причинами:
– разным числом атомов в молекуле. (например кислород и озон)
– образованием различных кристаллических форм.;(например алмаз, графит, карбин, фуллерен – это аллотропные модификации углерода)
Основные понятия химии
Раздел химии изучающий количественные отношения, в которых взаимодействуют друг с другом вещества, называется стехиометрией. В стехиометрии необходимо различать:
1) числа, стоящие перед формулами веществ в уравнениях химических реакций, называются стехиометрическими коэффициентами;
2) числа, стоящие справа внизу при символах химических элементов, характеризующие количественное содержание химического элемента в данном соединении, называются с техиометрическими индексами.
Все вещества состоят из атомов.
Наименьшая частица данного элемента, сохраняющая все его химические свойства, называется атомом.
Наименьшая частица данного вещества, обладающая его химическими свойствами, называется молекулой.
Каждый отдельный вид материи, обладающий при данных условиях определенными физическими свойствами, называется веществом.
Атомы и молекулы веществ характеризуются определенной физической массой:
mатома водорода = 1,66*10-24гmмолекулы воды = 2,99*10-23г
Производить расчеты таких величин неудобно. Поэтому в качестве единицы измерения выбирают массу одного из атомов.
В настоящее время в качестве атомной единицы массы (а.е.м.) используют 1/12 массы атома углерода:
1 а.е.м. = m(C)/12 = 1,999*10-23/12 = 1,66*10-24г
1 а.е.м. = 1,66*10-24г
 Относительная атомная масса элемента Ar – величина, равная отношению средней массы атома естественного изотопического состава элемента к 1/12 массы атома изотопа углерода 12C.
Относительная атомная масса элемента Ar – величина, равная отношению средней массы атома естественного изотопического состава элемента к 1/12 массы атома изотопа углерода 12C.
Относительная молекулярная масса вещества Mr – величина, равная отношению средней массы молекулы естественного изотопического состава вещества к 1/12 массы атома изотопа углерода 12C.
 |
Количество вещества определяется числом частиц, из которых состоит данное вещество(атомов, молекул, ионов и др) и обозначается буквой n.
Моль — это количество вещества, содержащее столько частиц (молекул, атомов, ионов или др.), сколько атомов содержится в 12 граммах изотопа углерода 12C
(12 г/моль)/m(C) = (12 г/моль)/(1,993*10-23г) = 6,02*1023 моль-1 = NA– число Авогадро
Число частиц рассчитывают по формуле:
N = n×NA
Массу атома или молекулы находят делением молярной массы на постоянную Авогадро:
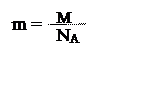 |
Молярная масса – это величина, равная отношению массы вещества (m) к количеству вещества (n): (М, г/моль)

Она численно равна относительной атомной массе Аr или Мr этого вещества.
Способность атомов соединяться с другими атомами в определенных соотношениях называется валентностью (В).
Основные законы химии
1. Закон сохранения массы веществ и энергии (М.В.Ломоносов, 1748). Во Франции этот же закон открыл в 1789 г. франц. Ученый Лавуазье.
Суммарные массы веществ и суммарные энергии до реакции равны суммарным массам веществ и суммарным энергиям после реакции.
В 1905 г. А. Энштейн показал, что между массой тела (m) и его энергией существует связь, выражаемая соотношением
Е = mс 2 уравнение Энштейна, с – скорость света в вакууме (≈ 3·10 8 м/с).
Всякая реакция сопровождается либо выделением энергии, либо поглощением. Выделение 1 ккал. уменьшает массу на 5·10-11 г.
Масса и энергия являются характеристиками материи, и общий закон Ломоносова носит название закона неуничтожаемости материи.
Дата добавления: 2015-02-16; просмотров: 68 | Поможем написать вашу работу | Нарушение авторских прав |