
|
Читайте также: |
Под пассивностью понимают состояние повышенной коррозионной стойкости металла или сплава, вызванное торможением процесса перехода ион-атомов металла в электролит.
В некоторых случаях при электрохимической коррозии величина коррозионного тока после замыкания цепи быстро падает и через определенное время становится постоянной, что объясняется уменьшением разности значений потенциалов. Такое изменение потенциалов в результате протекания тока называется поляризацией, а вещества, уменьшающие поляризацию, называются деполяризаторами.
Для объяснения явления пассивности предложено несколько различных теорий:
1. Анодная поляризация.
В зависимости от причин, вызывающих анодную поляризацию, различают три основных случая.
Концентрационная поляризация. Этот вид анодной поляризации вызывается небольшой скоростью диффузии ионов металла в растворе электролита, из-за чего образуется повышенная концентрация ионов в при анодной зоне.
Перенапряжение ионизации металла. Если при протекании анодного процесса

выход ионов металла в раствор не поспевает за отводом электронов, потенциал металла сдвигается в положительную сторону.
Анодная пассивность, которая заключается в образовании пассивных пленок на поверхности металла. Анодный процесс из-за наступления явления анодной пассивности резко тормозится. Этим можно объяснить достаточно высокую коррозионную стойкость алюминия и нержавеющих сталей в растворах азотной кислоты и в аэрированных растворах солей. Защитные фазовые пленки на аноде могут образовываться как результат отложения на поверхности металла труднорастворимых соединений этого металла.
2. Катодная поляризация.
Эта поляризация обусловливается перенапряжением катодной реакции, т. е. недостаточной скоростью подвода или отвода начальных либо конечных продуктов реакции на катоде. Возможны следующие основные виды катодной деполяризации:
а) деполяризация ионами;
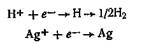
б) разряд катионов (ионов водорода или благородных металлов):
в) восстановление нейтральных молекул:

В пассивированном состоянии металл облагораживается, становится коррозионно стойким. Переход металла в пассивное состояние сопровождается изменением электродного потенциала. Например, железо в активном состоянии имеет электродный потенциал от —0,5 до —0,2 в, а в пассивном— от +0,2 до +1 в, потенциал хрома с —0,2 —0,6 в повышается до +0,8 +1 в. Следовательно, в пассивном состоянии металл имеет более положительный потенциал, а в активном — более отрицательный потенциал.
В пассивное состояние могут переходить такие металлы, как железо, хром, никель, алюминий, вольфрам, кобальт и др. Для перевода в пассивное состояние эти металлы погружают на некоторое время в раствор сильных окислителей, например в раствор хромового ангидрида, хромпика и др.; для алюминия хорошим пассиватором является HNO3. В настоящее время для изделий из алюминия и его сплавов широко применяется электролитический способ пассивирования (так называемое анодирование), при котором также образуется тончайшая защитная окисная пленка.
Некоторые металлы, например хром и алюминий, легко пассивируются кислородом воздуха, в том числе растворенным в электролите. Такие металлы называют самопассивирующимися, так как они способны восстанавливать свое пассивное состояние даже при повреждении окисной пленки,
Таким образом, пассивность является ценным свойством металлов и ее широко используют для повышения коррозионной стойкости металлических деталей.
Дата добавления: 2015-09-11; просмотров: 134 | Поможем написать вашу работу | Нарушение авторских прав |