
Читайте также:
|
Ответ:
Бензол C6H6 – родоначальник ароматических углеводородов.
Ароматические углеводороды (Арены) – это органические соединения, в молекулах которых имеется одно или несколько бензольных колец. Бензольное кольцо, или ядро, – циклическая группа атомов углерода с особым характером связей.
Общая формула - CnH2n-6
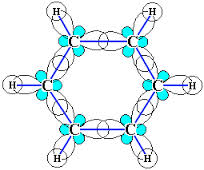
Каждый из шести атомов углерода в его молекуле находится в состоянии sp2 –гибридизации и связан с двумя соседними атомами углерода и атомом водорода тремя σ-связями. Валентные углы между связями С-С равны 120°. Таким образом, скелет σ-связей представляет собой правильный шестиугольник, в котором все атомы углерода и σ-связи С-С и С-Н лежат в одной плоскости:
Первую структурную формулу бензола предложил в 1865 г. немецкий химик Ф.А.Кекуле:

Атомы С в молекуле бензола образуют правильный плоский шестиугольник, хотя часто его рисуют вытянутым.
Приведенная формула правильно отражает равноценность шести атомов С, однако не объясняет ряд особых свойств бензола. Например, несмотря на ненасыщенность, он не проявляет склонности к реакциям присоединения: не обесцвечивает бромную воду и раствор перманганата калия, т.е. ему не свойственны типичные для непредельных соединений качественные реакции.
В структурной формуле Кекуле – три одинарные и три двойные чередующиеся углерод-углеродные связи. Но такое изображение не передает истинного строения молекулы. В действительности углерод-углеродные связи в бензоле равноценны. Это объясняется электронным строением его молекулы.
Каждый атом С в молекуле бензола находится в состоянии sp2-гибридизации. Он связан с двумя соседними атомами С и атомом Н тремя σ -связями. В результате образуется плоский шестиугольник, где все шесть атомов С и все σ -связи С–С и С–Н лежат в одной плоскости (угол между связями С–С равен 120o).
Третья p-орбиталь атома углерода не участвует в гибридизации. Она имеет форму гантели и ориентирована перпендикулярно плоскости бензольного кольца. Такие p-орбитали соседних атомов С перекрываются над и под плоскостью кольца.

Все связи С-С в бензоле равноценны, их длина составляет 0,140 нм, что соответствует промежуточному значению между длиной простой связи (0,154 нм) и двойной (0,134 нм). Это означает, что в молекуле бензола между углеродными атомами нет чисто простых и двойных связей, а все они выровнены (делокализованы). Поэтому структурную формулу бензола изображают в форме правильного шестиугольника (σ-скелет) и кружка внутри него, обозначающего делокализованные π-связи:

Формулу Кекуле также нередко используют, но при этом учитывается, что она лишь условно передает строение молекулы.
Гибридизация орбиталей — гипотетический процесс смешения разных (s, p, d, f) орбиталей центрального атома многоатомной молекулы с возникновением одинаковых орбиталей, эквивалентных по своим характеристикам.
Дата добавления: 2015-09-11; просмотров: 168 | Поможем написать вашу работу | Нарушение авторских прав |