
Читайте также:
|
1. Суворов -… 2. Иван Четвертый - … 3. Партийная кличка И.Джугашвили. 4. Святополк-…5. Дмитрий -... 6. Екатерина Вторая - …7. Алексей Михайлович - … 8. Алексей Пешков. 9. Александр Ярославич - …10. Партийная кличка Льва Бронштейна. 11. Мстислав - … 12. Партийная кличка Владимира Ульянова. 13. Ярослав - … 14. Лжедмитрий Второй – «… вор». 15. Николай Второй - … 16. Григорий Отрепьев. 17.Алексндр Второй - …18. Потемкин - …
По 1 баллу за каждое правильно названное прозвище (псевдоним).
Перечень обязательных инструкций, нормативной и технической документации.
Таблица №20
| № п/п | Наименование документа | Индекс документа |
| 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. 12. 13. 14. | Федеральный закон «О промышленной безопасности опасных производственных объектов». Правила промышленной безопасности для нефтеперерабатывающих производств. Правила пожарной безопасности в Российской Федерации. Правила пожарной безопасности при эксплуатации нефтеперерабатывающих прендприятий. Методические рекомендации по разработке технологического регламента на производство продукции нефтеперерабатывающей промышленности. Методические указания о порядке разработки плана локализации и ликвидации аварийных ситуаций (ПЛАС) на химико-технологических объектах. Временные руководящие указания по эксплуатации и ремонту систем аварийной сигнализации, блокировки и противоаварийной защиты на предприятиях. Положение о планово-предупредительном ремонте пневматических исполнительных механизмов систем автоматического регулирования. ГСИ. Проверка средств измерений. Организация и порядок проведения. ГСИ. Порядок осуществления государственного метрологического надзора за выпуском, состоянием и применением средств измерений, аттестованными методиками выполнения измерений, эталонами и соблюдения метрологических правил и норм. Правила устройства и безопасной эксплуатации технологических трубопроводов. Правила устройства электроустановок. Общие правила взрывобезопасности для взрывопожароопасных химических, нефтехимических и нефтеперерабатывающих производств. Правила устройства и безопасной эксплуатации сосудов, работающих под давлением. | №116-ФЗ 21.07.1997г. ПБ-09-563-03 ППБ-01-03 ППб-79 №4453 от 25.04.03г. - - ПР 50.2.006-94 ПР 50.2.002.-94 ПБ 03-585-03 ПУЭ ПБ 09-540-03 ПБ 03-576-03 |
| Продолжение таблицы №20 | ||
| 15. 16. 17. 18. 19. 20. 21. 22. 23. 24. 25. 26. 27. 28. 29. 30. 31. | Правила защиты от статического электричества в производствах химической, нефтехимической и нефтеперерабатывающей промышленности. Положение о порядке производства строительно-монтажных работ на территории ОАО «ЛУКОЙЛ – Нижегороднефтеоргсинтез» сторонними организациями. Положение о порядке проведения огневых работ на объектах АО. Перечень специальностей, которым необходимо иметь группы по электробезопасности. Положение по присвоению группы по электробезопасности. Стандарт предприятия. Управление несоответствующей продукцией. Стандарт предприятия. Порядок разработки технологической документацией. Стандарт предприятия. Контроль соблюдения технологической дисциплины. Стандарт предприятия. Идентификация и прослеживаемость. Стандарт предприятия. Управление процессами производства смазочных масел, парафинов, присадок к маслам. Требования к установке сигнализаторов и газоанализаторов. Определение категорий помещений и зданий по взрывопожарной и пожарной опасности. Правила технической эксплуатации трубчатых печей нефтеперерабатывающих и нефтехимических предприятий. Система технического обслуживания, ремонта и контроля технического состояния оборудования и установок дочерних нефтеперерабатывающих обществ ОАО «ЛУКОЙЛ». Инструкция по выбору прокладок при ремонте технологического оборудования Общие санитарно-гигиенические требования к воздуху рабочей зоны. Предельно допустимые концентрации(ПДК) вредных веществ в воздухе рабочей зоны. | - - - 2003г. - СТП СМК-30 СТП СМ-03 СТП СМК-24 СТП СМК-44 СТП СМК-35 ТУ ГАЗ-86 НПБ 105-03 ТП 01-88 СТП-01-021-01 М-150 ГОСТ 12.1.005-88 ГН 2.2.5.1313-03 |
| Продолжение таблицы №20 | ||
| 32. 33. 34. 35. 36. 37. 38. 39. 40. 41. 42. 43. 44. 45. 46. 47. | Сосуды работающие под давлением. Клапаны предохранительные. Порядок эксплуатации, ревизии и ремонта пружинных предохранительных клапанов в дочерних нефтегазодобывающих, нефтеперерабатывающих, нефтехимических, газоперерабатывающих обществах и обществах нефтепродуктообеспечения ОАО «ЛУКОЙЛ». Автоматизация технологических процессов. Положение о порядке организации обслуживания приборов автоматического контроля за состоянием атмосферы производственных помещений и наружных установок Правила устройства и безопасной эксплуатации трубопроводов пара и горячей воды Должностные инструкции. Инструкция о мерах пожарной безопасности в ОАО «ЛУКОЙЛ – Нижегороднефтеоргсинтез». Инструкция по газобезопасности. Инструкция по организации безопасного проведения газоопасных работ и работ внутри аппаратов на объектах ОАО «ЛУКОЙЛ – Нижегороднефтеоргсинтез». Инструкция о порядке безопасного проведения ремонтных работ в ОАО «ЛУКОЙЛ – Нижегороднефтеоргсинтез». Инструкция по охране труда для пользователей при работе на персональных электронно-вычислительных машинах (ПЭВМ) и копировально-множительных аппаратах (КМА). Инструкция по эксплуатации и техническому обслуживанию огнетушителей в ОАО «ЛУКОЙЛ – Нижегороднефтеоргсинтез». Инструкция по безопасному выполнению работ по постановке и уборке вагонов под погрузку и выгрузку на железнодорожных путях ОАО «ЛУКОЙЛ – Нижегороднефтеоргсинтез». Инструкция по безопасной эксплуатации и обслуживанию резервуаров ОАО "ЛУКОЙЛ-Нижегороднефтеоргсинтез". Инструкция по охране труда для уборщиков производственных и служебных помещений. Инструкция по организации безопасного производства работ на высоте на объектах ОАО «ЛУКОЙЛ – Нижегороднефтеоргсинтез». | ГОСТ 12.2.085-82 РД-01-601-2002 ГОСТ 21.404-85 - ПБ 10-573-03 - ИБ-01-2003 ИБ-02-2005 ИБ-3-2004 ИБ-05-2006 ОТ-06-2003 ИБ-9-2003 ИБ-10-2005 ИБ-11-2004 ОТ-14-2006 ИБ-15-2004 |
| Продолжение таблицы №20 | ||
| 48. 49. 50. 51. 52. 53. 54. 55. 56. 57. 58. 59. 60. 61. | Инструкция по организации безопасного проведения огневых работ на объектах ОАО «ЛУКОЙЛ-Нижегороднефтеоргсинтез». Инструкция о порядке безопасного производства земляных работ на территории ОАО "ЛУКОЙЛ- Нижегороднефтеоргсинтез " Инструкция по эксплуатации, ревизии и ремонту пружинных предохранительных клапанов ОАО «ЛУКОЙЛ-Нижегороднефтеоргсинтез». Инструкция по эксплуатации и техническому обслуживанию аппаратов воздушного охлаждения ОАО «ЛУКОЙЛ-Нижегороднефтеоргсинтез». Инструкция по гидравлическому испытанию сосудов, эксплуатирующихся на объектах ОАО «ЛУКОЙЛ-Нижегороднефтеоргсинтез». Инструкция по пневматическому испытанию сосудов, эксплуатирующихся на объектах ОАО «ЛУКОЙЛ-Нижегороднефтеоргсинтез». Инструкция по испытанию на герметичность сосудов, эксплуатирующихся на объектах ОАО «ЛУКОЙЛ-Нижегороднефтеоргсинтез». Инструкция по эксплуатации и техническому обслуживанию вентиляционных систем. Инструкция по безопасной эксплуатации и техническому обслуживанию взрывозащищенных вентиляторов. Инструкция по проведению пневматического испытания технологических трубопроводов на прочность, плотность и дополнительных испытаний на герметичность на объектах ОАО «ЛУКОЙЛ-Нижегороднефтеоргсинтез». Инструкция по эксплуатации и техническому обслуживанию центробежных насосов ОАО «ЛУКОЙЛ-Нижегороднефтеоргсинтез». Инструкция по эксплуатации и техническому обслуживанию поршневых насосов ОАО «ЛУКОЙЛ-Нижегороднефтеоргсинтез». Инструкция по эксплуатации и техническому обслуживанию шестерёнчатых и винтовых насосов ОАО «ЛУКОЙЛ-Нижегороднефтеоргсинтез». Инструкция по эксплуатации и техническому обслуживанию технологических трубопроводов с давлением до 10 МПа (100 кгс/см2) на объектах ОАО «ЛУКОЙЛ-Нижегороднефтеоргсинтез». | ИБ-16-2005 ИБ-22-2006 М-001 М-104 М-106 М-107 М-109 М-110 М-114 М-116 М-121 М-122 М-123 М-127 |
| Продолжение таблицы №20 | ||
| 62. 63. 64. 65. 66. 67. 68. 69. 70. 71. 72. 73. | Инструкция по эксплуатации запорных клапанов типа КЗ 21216 (15с68нж) на объектах ОАО «ЛУКОЙЛ-Нижегороднефтеоргсинтез». Инструкция по техническому обслуживанию сосудов, эксплуатирующихся на объектах ОАО «ЛУКОЙЛ-Нижегороднефтеоргсинтез» Инструкция по эксплуатации и технике безопасности передвижной установки высокого давления. Инструкция по проведению вибродиагностических измерений центробежного динамического оборудования на объектах ОАО «ЛУКОЙЛ-Нижегороднефтеоргсинтез». Инструкция по обслуживанию контрольно-измерительных приборов на технологических установках ОАО «ЛУКОЙЛ-Нижегороднефтеоргсинтез». Инструкция по ведению записей в вахтовом журнале, режимном (операторном) листе, по замерам уровня в резервуарах на технологических объектах ОАО «ЛУКОЙЛ-Нижегороднефтеоргсинтез». Инструкция о порядке отбора и проведения анализа проб воздушной среды в подразделениях ОАО «ЛУКОЙЛ-Нижегороднефтеоргсинтез». Инструкция по взаимодействию персонала ОАО «ЛУКОЙЛ-Нижегороднефтеоргсинтез» и ЗАО «Нефтехим» по обслуживанию технологических схем и узлов переключений при перекачке продукции. Положение о порядке организации обслуживания приборов автоматического контроля за состоянием атмосферы производственных помещений и наружных установок ОАО «ЛУКОЙЛ-Нижегороднефтеоргсинтез». Инструкция о порядке учёта отказов, неисправностей контрольно-измерительных приборов, автоматики и их устранение на объектах ОАО «ЛУКОЙЛ-Нижегороднефтеоргсинтез». Инструкция по эксплуатации, техническому обслуживанию, ремонту и проверке схем сигнализации, блокировок и противоаварийной автоматической защиты технологических процессов. Инструкция по монтажу и эксплуатации показывающих манометров, мановакуумметров и вакуумметров на объектах ОАО «ЛУКОЙЛ-Нижегороднефтеоргсинтез». | М-127а М-128 М-129 б/н Т-101 Т-102 Т-104 Т-105 П-1/К-2005 К-101 К-103 К-107 |
| Продолжение таблицы №20 | ||
| 74. 75. 76. 77. 78. 79. 80. 81. 82. 83. 84. 85. 86. 87. | Инструкция по эксплуатации систем теплоснабжения подразделений ОАО «ЛУКОЙЛ-Нижегороднефтеоргсинтез». Инструкция по эксплуатации переносных аккумуляторных светильников типа СГВ-2, СГД-5. Инструкция по эксплуатации, подготовке к ремонту и пуску установки гидроочистки масел и парафина Г-24. Инструкция о мерах пожарной безопасности на установке гидроочистки масел и парафина Г-24 производства смазочных масел ОАО «ЛУКОЙЛ-Нижегороднефтеоргсинтез». Инструкция по охране труда для операторов технологической установки гидроочистки масел и парафина Г-24 цеха по производству товарных масел и парафина производства смазочных масел в ОАО «ЛУКОЙЛ-Нижегороднефтеоргсинтез». Эксплуатация АРМ распределенной системы управления "SIMATIC" установки Г-24/1 ПСМ. Инструкция по эксплуатации и техническому обслуживанию насосов 9МГР-61, ХТР-12/100, НБ-50, НДБ-2,5 Р 5000/10 установки Г-24/1 ПСМ. Инструкция по эксплуатации и техническому обслуживанию центрифужного фильтра ZHF-SP 25KLK B2 на установке гидроочистки масел и парафина Г-24/1 производства смазочных масел Инструкция по эксплуатации и техническому обслуживанию компрессора 5Г-300/42-60 установки Г-24 ПСМ. Инструкция по эксплуатации и техническому обслуживанию водокольцевых насосов установки Г-24. Положение по переводу центробежного динамического оборудования с графика ППР на ремонт по техническому состоянию методом вибродиагностики и проведению измерений на объектах предприятия. Выписка из технологического регламента. План локализации и ликвидации аварийных ситуаций (ПЛАС). Инструкция по взаимодействию между ОАО «ЛУКОЙЛ-Нижегороднефтеоргсинтез» и ООО «ЭКОИН» при эксплуатации систем водоснабжения и канализации и обращению с отходами производства и потребления. | Э-102 Э-115 Т-51/ПСМ ИБ-01/ПСМ-2005 ОТ-07/14-2004 К-04 М-108/13 М-108/14 М-109/14 М-111/13 Б/н |
| Продолжение таблицы №20 | ||
| 88. 89. 90. 91. 92. 93. 94. 95. 96. 97. 98. 99. | Инструкция о порядке обращения с отходами производства и потребления в ОАО «ЛУКОЙЛ-Нижегороднефтеоргсинтез». Система управления охраной труда. Инструкция по оказанию первой помощи при несчастных случаях на производстве. Правила внутреннего трудового распорядка для рабочих и служащих ОАО «ЛУКОЙЛ-Нижегороднефтеоргсинтез». Приложение №9 к "Правилам внутреннего трудового распорядка для рабочих и служащих ОАО “ЛУКОЙЛ-Нижегороднефтеоргсинтез”, определяющих время и продолжительность перерывов для отдыха и приема пищи сменного персонала производства смазочных масел. Положение о внутриобъектовом и пропускном режиме в ОАО «ЛУКОЙЛ-Нижегороднефтеоргсинтез». Выписка из “Правил технической эксплуатации эл. установок потребителей”, утверждённых Минэнерго России за № 6 от 13.01.03., “Межотраслевых правил по охране труда (правил безопасности) при эксплуатации эл. установок”, утверждённых Министерством энергетики России приказом № 163 от 27 декабря 2000 г., с изменениями и дополнениями, “Правил устройств эл. установок”, 6-е издание, переработанное и дополненное, с изменениями, обязательных для знания не электротехнического персонала, имеющих I и II группу по электробезопасности подразделений ОАО “ЛУКОЙЛ-Нижегороднефтеоргсинтез”. Политика ОАО «ЛУКОЙЛ-Нижегороднефтеоргсинтез» в области промышленной безопасности и охраны труда. Экологическая политика ОАО «ЛУКОЙЛ-Нижегороднефтеоргсинтез». Политика ОАО «ЛУКОЙЛ-Нижегороднефтеоргсинтез» в области качества. Экономическая политика ОАО «ЛУКОЙЛ-Нижегороднефтеоргсинтез». Политика управления персоналом ОАО «ЛУКОЙЛ-Нижегород-нефтеоргсинтез». | Б/н Б/н |
Стехиометрия реакций и материальные расчеты
Первичной основой учения о химических превращениях веществ является стехиометрия, на которой базируются все количественные соотношения при химических реакциях.
Слово стехиометрия (от др.- греч. στοιχεῖον = «элемент» + μετρέω = «измерять») – буквально означает измерение элементов некоторого ряда или серии – раздел химии о соотношениях реагентов в химических реакциях. Обычно оно применяется ко всем способам вычислений, касающихся компонентов химической системы. Мы будем использовать его там, где приходится иметь дело со структурой арифметических соотношений между веществами, участвующими в химическом процессе. По существу, стехиометрия – это бухгалтерия материальных компонентов химической системы.
Изменения состава реагирующей смеси не случайны, а определяются двумя различными причинами. Первая причина — внешняя: подача или удаление вещества из системы; вторая причина — внутренняя: изменения, вызванные химической реакцией. В то время как перенос вещества в пространстве описывается уравнениями материального баланса, соответствующими определенному типу реактора, внутренние изменения зависят только от самой химической реакции и поэтому одинаковы для реакторов всех типов.
При химической реакции происходит количественное и качественное изменение состава участвующих в реакции молекул (разрушение исходных и образование новых) за счет перераспределения атомов, образующих молекулы реагентов. При этом атомы сохраняют свои индивидуальные свойства (например, масса, заряд ядра и т. п.) и образуют лишь вполне определенные связи между собой, определяющиеся структурой и зарядом их электронных оболочек. Иными словами, атомы образуют между собой лишь дискретные, целочисленные ассоциации (молекулы, радикалы, ионы) с учетом их валентных состояний.
С другой стороны, указанное постоянство атомов обеспечивает сохранение массы реагирующей системы. Эти очевидные и ставшие тривиальными положения, однако, чрезвычайно ценны для понимания динамики химических превращений. Учет этих связей особенно полезен при проведении кинетических исследований сложных реакционных систем.
Стехиометрия накладывает ограничения на возможные изменения состава реагирующей смеси.
В технике количество вещества чаще всего выражают через их массу mi, измеряемую в килограммах, тоннах и других единицах. В соответствии с «Законом эквивалентов», при химических реакциях вещества взаимодействуют в эквивалентных соотношениях. Однако, значения эквивалентов величины, строго говоря, не постоянные, и зависят от конкретной реакции, в которой это вещество участвует. Например, KMnO4 и K2SO3 в реакциях в разных средах реагируют различным образом:
- в кислой среде: 2KMnO4 + 5K2SO3 + 3H2SO4 = 2MnSO4 + 6K2SO4 + 3H2O
- в нейтральной среде: 2KMnO4 + 3K2SO3 + H2O = 2MnO2 + 3K2SO4 + 2KOH
- в щелочной среде: 2KMnO4 + K2SO3 + 2KOH = 2 K2MnO4 + K2SO4 + H2O
Значение г-эквивалента KMnO4 в этих реакциях равно 31.6 г, 79.0 г и 158.0 г, соответственно.
Более удобны мольные количества. Напомним, что 1 г-моль любого вещества – содержит 6·1023 молекул (число Авогадро). При этом для выполнения закона эквивалентов, вводят стехиометрические коэффициенты.
В химии для материальных расчетов используют такие величины как моль или кмоль. Они связаны с массой соотношением
 или
или 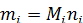 [2.1]
[2.1]
где Мi – молекулярная масса вещества (г/моль или кг/кмоль), ni – количество молей вещества.
Мольные количества вещества ni вполне подходят для характеристики периодических процессов. В условиях проточных процессов, когда вещества подают и выводят из реактора непрерывно, более приемлемой характеристикой является мольный поток, который для стационарного режима процесса выражается уравнением
 моль(кмоль)/в ед. времени[2.2]
моль(кмоль)/в ед. времени[2.2]
где t – промежуток времени, в течение которого подают ni моль вещества.
С точки зрения стехиометрии все химические реакции подразделяют на простые и сложные.
Простые реакции характеризуются тем, что при них протекает единственное необратимое превращение и не образуется иных стабильных продуктов, кроме записанных в уравнении реакции:
va A + vb B = vr R + vs S (I)
Для каждой простой реакции можно написать следующие равенства, являющиеся основным соотношением ее баланса:

 [2.3]
[2.3]
где vi – стехиометрический коэффициент вещества J. Эти равенства справедливы при условии, что стехиометрические коэффициенты расходуемых веществ берутся со знаком минус, а для образующихся – со знаком плюс. При этом величина n или F всегда положительна, инвариантна в отношении участников реакции и называется полнотой реакции.
Из равенств [2.3] вытекают уравнения материального баланса простых реакций
 [2.4]
[2.4]
по которым, зная начальные условия и n или F для одного из веществ, по формулам [2.3] находят полноту реакции и затем по уравнениям [2.4] мольные количества или мольные потоке всех других компонентов реакции.
Пример.
Полагая, что реакция диспропорционирования циклогексена с образованием бензола и циклогексана
3С6Н10 = 2С6Н12 + С6Н6
является простой, вычислить ni, если известно, что
 = 12 моль,
= 12 моль,  =
=  = 0 и
= 0 и  = 3 моль.
= 3 моль.
По уравнению [2.3] находим:

n = 3
Тогда по уравнению [2.4] имеем:
 = 0 + 2 · 3 = 6 моль
= 0 + 2 · 3 = 6 моль
 = 0 + 1 · 3 = 3 моль
= 0 + 1 · 3 = 3 моль
Из равенств [2.3] следует, что мольное соотношение образующихся или расходуемых веществ, при простых реакциях, постоянно и равно соотношению стехиометрических коэффициентов этих веществ в уравнении реакции:
ni - ni,0 = vi/vA· (nA – nA,0) или Fi - Fi,0 = vi/vA· (FA – FA,0)
В координатах Δni от ΔnA или ΔFi от ΔFA для любого компонента простой реакции должна получиться прямая, тангенс угла наклона которой равен vi/vA (рис. 2).
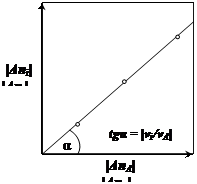
Рис. 2.2. Изменение мольного соотношения
веществ при простых реакциях
Этим путем можно экспериментально убедиться, что изучаемая реакция – простая.
Сложные реакции состоят из ряда простых реакций. К ним принадлежат:
- обратимые реакции
vA A + … ↔ vR R + …
- параллельные превращения
v1,A A + … → vR R + …
v2A A + … → vS S + …
- последовательные превращения,
vA A + … → vB B + … → vC C
а также более сложные в стехиометрическом отношении системы, включающие сочетания этих трех типов сложных реакций.
Среди веществ, участвующих в сложных реакциях, различают исходные реагенты и продукты. Среди исходных реагентов один – обычно основной (более дорогостоящий или определяющий основную схему превращений). В дальнейшем, будем обозначать его через А. Из продуктов реакции один является целевым, ради которого реализуется весь процесс. Целевой продукт обозначим буквой В. Остальные продукты реакции называют побочными. Соответственно этому реакция образования целевого продукта называется целевой, а остальные – побочными.
Необходимо отметить, что побочные продукты могут образовываться не только в побочных реакциях, но и быть продуктами целевой.
При анализе известной системы сложных реакций, прежде всего, необходимо определить число стехиометрически независимых превращений, уравнения которых нельзя получить комбинацией уравнений других реакций (сложением, вычитанием, умножением стехиометрических коэффициентов на постоянные множители). В большинстве случаев это легко сделать последовательным исключением стехиометрически зависимых реакций. Так, при обратимом превращении уравнение обратной реакции легко получить, умножив уравнение прямой реакции на минус единицу. Следовательно, в этом случае имеется только одно независимое превращение.
Рассмотрим систему сложных реакций дегидратации этанола
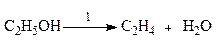


исключив реакцию -2 (как обратную второй) и реакцию 3 (уравнение которой можно получить вычитанием уравнения 2 из уравнения 1, находим, что система имеет лишь две независимые реакции.
В более сложных случаях для определения числа (R) стехиометрически независимых превращений используют методы матричной алгебры, составляя стехиометрическую матрицу, строки и столбцы которой соответствуют определенным веществам и реакциям. Для предыдущей системы стехиометрическая матрица будет такой:
| В = | -1 | |||
| -2 | ||||
| -1 | -1 | |||
| -1 |
Оказывается, что ранг стехиометрической матрицы равен числу независимых реакций. Ранг представленной матрицы равен 2.
Одновременно с числом независимых реакций определяют равное ему число так называемых ключевых веществ, по которым можно полностью охарактеризовать материальный баланс системы. В простой реакции ключевое вещество только одно (например, циклогексен из предыдущего примера). В сложных системах выбор независимых реакций и ключевых веществ взаимосвязан и определяется тем, чтобы в каждой независимой реакции участвовало хотя бы одно ключевое вещество и в то же время выбранные ключевые вещества участвовали бы только в одной или в некотором минимуме независимых реакций. Так, для дегидратации этанола выгодно выбрать в качестве независимых реакций 1 и 2, а в качестве ключевых веществ — этилен и диэтиловый эфир. Выбор ключевых веществ зависит также от простоты и точности их аналитического определения.
После анализа сложной системы превращений, выбора независимых реакций и ключевых веществ легко провести ее материальный расчет. Для каждой из независимых реакций по аналогии с выражением [2.3] можно записать уравнения полноты реакции


где индекс i соответствует веществу, а индекс j - реакции. Тогда, имея в виду, что каждое из веществ может участвовать в нескольких реакциях (Δ ni =ΣΔ nij), получим:
 [2.5]
[2.5]
Зная начальные условия и ni (или Fi) для ключевых веществ, находим вначале по уравнениям [2.5] полноту реакций nj или Fj и затем полный состав реакционной массы. Отметим, что при обратимых реакциях с единственным независимым превращением и одним ключевым веществом справедливы уравнения баланса, выведенные ранее для простых реакций, в том числе соотношения, иллюстрированные на рис. 2.2.
Пример.
При дегидратации этанола его начальный мольный поток Fc2h5он,0 = 1000 кмоль/ч,
Fc2h4=300 кмоль/ч и F(c2h5)2O = 200 кмоль/ч.
Рассчитать материальный баланс процесса.
Решение.
При независимых реакциях 1 и 2 (см. ранее) имеем:
Fc2h4 = 0 + 1F1 F1 = 300
F(c2h5)2O = 0 + 1F2 F2 = 200
Тогда
Fc2h5он = 1000 – 1*300 – 2*200 = 300 кмоль/ч
Fh2O = 0 + 1*300 + 1*200 = 500 кмоль/ч
На основе этого расчета составляется таблица материального баланса, в которой сопоставляются взятые и полученные количества веществ. Например, для предыдущего расчета получим:
| Наименование компонента | Подано | Получено | ||
| кмоль/ч | кг/ч | кмоль/ч | кг/ч | |
| Этанол | 1 000,0 | 46 000 | 300,0 | 13 800 |
| Этилен | 0,0 | 0,0 | 300,0 | 8 400 |
| Диэтиловый эфир | 0,0 | 0,0 | 200,0 | 14 800 |
| Вода | 0,0 | 0,0 | 500,0 | 9 000 |
| Итого: | 1 000,0 | 46 000 | 1 300,0 | 46 000 |
При балансовых опытах или подведении фактического материального баланса установки обычно наблюдается небольшое расхождение между суммами взятых и полученных веществ. Это объясняется неточностью анализов и неучтенными потерями. Материальные расчеты удобно проводить по независимым суммарным реакциям образования ключевых веществ из исходных реагентов. В рассмотренном выше примере они совпадают с соответствующими простыми реакциями, но в других случаях
бывает не так. Например, при этилировании бензола протекают следующие простые реакции:

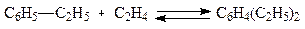

Стехиометрический анализ показывает, что из шести простых
реакций две являются независимыми. Столько же имеется и ключевых веществ, за которые можно принять два вещества - этилбензол и диэтилбензол. Суммарные реакции их образования из исходных реагентов таковы:


Одна из них совпадает с соответствующей простой реакцией, а
другая не совпадает и имеет иные стехиометрические коэффициенты, которые обозначим v′i. Выведенное ранее уравнение баланса [2.5] для сложных реакций применимо и для суммарных реакций. Поэтому дальнейший расчет при заданных начальных условиях и Fi (ni) для ключевых веществ проводится аналогично.
Уравнение [2.5] для суммарных реакций образования ключевых веществ служит для составления баланса по исходным реагентам, который часто необходим при исследовании или расчете процесса. Когда каждое из ключевых веществ образуется только по одной суммарной реакции, имеем:

Например, для разбираемого процесса этилирования бензола получим:


Безразмерные характеристики материального баланса реакций.
Как уже было сказано выше, в химии и химической технологии большое значение имеют безразмерные характеристики материального баланса – степень конверсии (степень превращения), селективность и выход.
Степень конверсии (степень превращения, конверсия) – доля прореагировавшего исходного реагента относительно его начального количества. Степень превращения реагента показывает, насколько полно в химико-технологическом процессе используется исходное сырье.
Конверсия реагента A
 [2.6]
[2.6]
В примере дегидратации этанола степень его конверсии составляет:
ХROH = (1000 – 300):1000 = 0,70 или 70,0%
Чаще всего в химической реакции участвует не один, а два реагента (или даже больше). При этом обычно степень конверсии определяют по основному реагенту А, но она может быть рассчитана по каждому реагенту, причем в общем случае не обязательно получаются равные результаты.
Степени превращения реагентов A и B, участвующих в реакции (I):
 ;
; 
Необходимо помнить, что конверсия – это доля первоначального количества реагента, т. е. пределы изменения Хi определяются соотношением  .
.
Если один из реагентов (например, реагент В) взят в избытке, то всегда
Х В < 1, даже в том случае, когда Х A = 1.
Обычно при выборе первоначального состава реакционной смеси берут в избытке более дешевый реагент (например, воздух, воду и т. д.) с целью повышения степени использования более ценного сырья.
В разных процессах химической технологии степень конверсии
изменяется от 4÷5 до почти 100%. Из уравнения [2.6] следует:
 [2.7]
[2.7]
 [2.8]
[2.8]
Для простых и обратимых реакций, когда имеются единственное независимое превращение и одно ключевое вещество, степень конверсии – вполне достаточная характеристика материального баланса. Действительно, зная ni,0 (Fi,0) и ХA, легко рассчитать FA по уравнению [2.7], n (F) по формуле [2.3] и затем все ni (Fi) по уравнению [2.4]. Кроме того, для любой простой или обратимой реакции

в дополнение к соотношению [2.7] легко вывести зависимость ni (Fi) от nА,0 (FА,0) и степени конверсии основного реагента ХА:

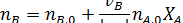

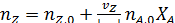
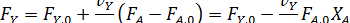

где | vA | - абсолютное значение стехиометрического коэффициента при реагенте А.
Не всегда возможно достичь полного использования реагента (т. е. условия X i = 1). Большинство химических реакций обратимы. Для обратимых реакций при заданных условиях их осуществления предельным является состояние химического равновесия.
Для сложных реакций, более одного ключевого компонента, степень конверсии показывает лишь долю прореагировавшего вещества, но не дает представления о направлениях его превращения, которое определяется селективностью и выходом.
Селективность — доля (или процент) превращенного исходного реагента, израсходованная на образование данного продукта. При этом всегда учитывают только химические превращения в реакторе, исключая какие-либо иные потери веществ (кроме их расходования на образование побочных продуктов). Другими словами, селективность можно определить как отношение количества полученного продукта к его теоретическому количеству, которое могло бы образоваться из превращенного реагента при отсутствии побочных реакций и потерь. Теоретическое количество легко рассчитать по суммарной реакции образования данного продукта из исходных реагентов, применяя к ней уравнения [2.3]:

Тогда получим выражение для селективности Ф
 [2.9]
[2.9]
в котором двойной индекс при Ф означает, что селективность определена для продукта i по основному реагенту А. Ее можно выразить и по другому реагенту. Когда исходное вещество является единственным или известно, по какому из реагентов определяется селективность, индекс А (или Y) может быть опущен.
Очевидно, что количество основного реагента, пошедшее на образование всех образующихся продуктов равно количеству затраченного основного реагента и, следовательно
 [2.10]
[2.10]
Так для ранее рассмотренного примера дегидратации этанола получим:


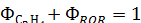
Селективность по целевому продукту показывает долю полезно использованного сырья; она является важной характеристикой катализаторов, условий проведения процесса и типа реакторного узла. На практике селективность по целевому продукту изменяется от 50÷60 до 100%, причем повышение селективности – одна из важнейших задач химической технологии.
Полная, или интегральная, селективность Ф – это отношение количества исходного реагента, расходуемого на целевую реакцию, к общему количеству исходного реагента, пошедшего на все реакции (и целевую, и побочные):

Мгновенной, или дифференциальной, селективностью Ф′ называют отношение скорости превращения исходных реагентов в целевой продукт к суммарной скорости расходования исходных реагентов;
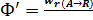
где w r(A→R) – скорость расходования реагента А по целевой реакции; w rA – суммарная скорость расходования реагента А.
Понятие дифференциальной (мгновенной) селективности имеет смысл только для параллельных реакций.
Выход – это далеко не однозначное понятие. Иногда под ним понимают абсолютное количество полученного продукта (в г, кг, моль и кмоль), но чаще выход выражают в долях единицы или в процентах на взятое сырье. Кроме того, выход применяют для характеристики систем разного масштаба – только реакционного аппарата (химический выход), какого-либо узла производства или технологической схемы в целом, когда учитывают не только расход сырья на химические реакции, но и различные потери (технологический выход). Далее мы будем применять понятие только химического выхода.
Химический выход равен мольному количеству полученного продукта i, отнесенному к его теоретическому возможному количеству. Следовательно, выражение для выхода легко получить из формулы [2.9] при ХА = 1:
 [2.11]
[2.11]
Выход можно рассчитывать и по второму реагенту, причем в литературе встречаются и другие обозначения выхода.
Объединяя формулы [2.9] и [2.11] получим, что выход равен произведению селективности на степень конверсии.
 [2.12] При этом сумма выходов ключевых веществ по основному реагенту А с учетом уравнения [2.10] равна степени конверсии этого реагента.
[2.12] При этом сумма выходов ключевых веществ по основному реагенту А с учетом уравнения [2.10] равна степени конверсии этого реагента.
 [2.13] Используя уравнение [2.11] мольные количества и мольные потоки можно выразить через их выходы.
[2.13] Используя уравнение [2.11] мольные количества и мольные потоки можно выразить через их выходы.

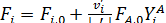 [2.14]
[2.14]

 [2.15]
[2.15]
Последние уравнения широко используются в химической кинетике и при расчете реакторов. Очевидно, что при расчете материальных балансов процесса все или часть исходных данных (за исключением ni,0 или Fi,0) может быть задана безразмерными характеристиками – степенью конверсии, селективностью или выходом. Тогда, используя выведенные уравнения, легко рассчитывают мольные количества или потоки всех веществ и составляют таблицу материального баланса.
Парциальные молярные балансы. На безразмерных характеристиках реакций основаны расчеты так называемых парциальных молярных балансов, составляемых на 1 моль основного исходного реагента А. При этом начальный состав смеси также выражают через безразмерные величины, а именно мольные соотношения других веществ, в том числе инертных, к основному реагенту А:
 [2.16]
[2.16]
Безразмерные формы уравнений баланса составляют по независимым суммарным реакциям, деля выражения полученные по формулам [2.5] на nА,0 или FА,0:


Здесь 
Величина  есть степень полноты или частная степень конверсии основного реагента по данной суммарной реакции, и обозначается как хj, изменяющаяся от 0 до 1. Если какое-либо ключевое вещество образуется только по этой реакции, то имеем
есть степень полноты или частная степень конверсии основного реагента по данной суммарной реакции, и обозначается как хj, изменяющаяся от 0 до 1. Если какое-либо ключевое вещество образуется только по этой реакции, то имеем

т.е. его выход равен степени полноты реакции. Следовательно, получаем уравнение парциального молярного баланса:  [2.17]
[2.17]
Рассчитаем парциальный молярный баланс реакции дегидратации этанола:

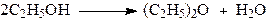
Согласно предыдущим расчетам, имеем:




Самостоятельная работа к лекции 2
1. Определить число независимых реакций
4NH3+5O2=4NO+6H2O
4NH3+3O2=2N2+6H2O
4NH3+6NO=5N2+6H2O
2NO+O2=2NO2
2NO=N2+O2
N2+2O2=2NO2
2. При окислении этилена протекают реакции

Составьте стехиометрическую матрицу, найдите число независимых реакций, выберите независимые реакции и ключевые вещества.
3. Для предыдущей реакции провести материальный расчет для условий:
начальный мольный поток этилена равен 150 кмоль/ч, степень его конверсии
0,40; селективность образования этиленоксида 0,70; мольное соотношение кислорода и этилена β = 0,60. Составьте таблицу материального баланса.
4. Для реакции из примера 2 составьте общие уравнения зависимости
мольных потоков веществ от начального мольного потока этилена, выходов этиленоксида и диоксида углерода.
Дата добавления: 2014-12-15; просмотров: 166 | Поможем написать вашу работу | Нарушение авторских прав |
|