
Читайте также:
|
Модель Резерфорда противоречила экспериментальным исследованиям, не позволяла определить спектральные закономерности, поэтому Бор выдвинул постулаты для описания поведения электрона в атоме.
1. Постулат: Постулат стационарных состояний: Атом может длительное время находиться в устойчивых стационарных состояниях, в которых он не излучает энергию. В стационарном состоянии обладает квантовым значением энергии.
2. Правило частот: Излучение и поглощение энергии атома происходит в момент скачкообразного перехода из одного стационарного состояния в другое.
Атомы излучают и поглощают энергию дискретными порциями (квантами).
Энергия кванта = разности энергий стационарных состояний.
Еγ= Е к- Еn
3. Правило квантования орбит: Стационарно разряженные орбиты в атоме находятся из условия:
mυrn=nħ
где m-масса электрона, υ- линейная скорость его движения, rn—радиус n орбиты
ħ=h/2π=1,05*10-34Дж*с
Бор, используя свои постулаты и планетарную модель Резерфорда, разработал количественную теорию атома водорода; рассчитал радиусы дозволенных орбит электрона; вычислил соответствующий им энергетический уровень.
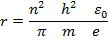
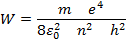
Бор не смог построить модели других атомов, кроме водорода.
Дата добавления: 2014-11-24; просмотров: 114 | Поможем написать вашу работу | Нарушение авторских прав |