
Читайте также:
|
Как известно, диффузия при более высокой температуре происходит быстрее. Из этого следует, что скорость перемещения молекул и температура глубоко взаимосвязаны между собой. Если увеличить температуру, то скорость движения молекул увеличится, если уменьшить – понизится.
Таким образом, делаем вывод: температура тела напрямую зависит от скорости перемещения молекул.
Горячая вода состоит из абсолютно таких же молекул, как и холодная. Разница между ними состоит лишь в скорости передвижения молекул.
Явления, которые имеют отношение к нагреву или охлаждению тел, изменению температуры, получили название тепловые. К ним можно отнести нагревание или охлаждение воздуха, плавку метала, таяние снега.
Молекулы, либо атомы, которые являются основой всех тел, находятся в бесконечном хаотичном движении. Количество подобных молекул и атомов в окружающих нас телах огромно. В объеме равном 1 см³ воды, содержится приблизительно 3,34 · 10²² молекул. Любая молекула имеет очень сложную траекторию движения. К примеру, частицы газа, передвигающиеся с большими скоростями в различных направлениях, могут сталкиваться как друг c другом, так и со стенками сосуда. Таким образом, они меняют свою скорость и опять продолжают движение.
Рисунок №1 демонстрирует беспорядочное движение частиц краски, растворенных в воде. 
Таким образом, делаем еще один вывод: хаотичное движение частиц, которые составляют тела, называют тепловым движением.
Хаотичность является важнейшей чертой теплового движения. Одним из самых главных доказательств движения молекул является диффузия и Броуновское движение. (Броуновское движение – движение мельчайших твердых частиц в жидкости под воздействием ударов молекул. Как показывает наблюдение, Броуновское движение не может прекратиться).
В жидкостях молекулы могут колебаться, вращаться и двигаться относительно других молекул. Если брать твердые тела, то в них молекулы и атомы колеблются около некоторых средних положениях.
В тепловом движении молекул и атомов участвуют абсолютно все молекулы тела, именно поэтому с изменением теплового движения меняется и состояние самого тела, его различные свойства. Таким образом, если повысить температуру льда то он начинает таять, принимая при этом уже абсолютно другую форму – лед становится жидкостью. Если же наоборот, понижать температуру, к примеру, ртути, то она изменит свои свойства и из жидкости, превратится в твердое тело. 
Температура тела напрямую зависит от средней кинетической энергии молекул. Делаем очевидный вывод: чем выше температура тела, тем больше средняя кинетическая энергия его молекул. И, наоборот, при понижении температуры тела, средняя кинетическая энергия его молекул уменьшается.
№19
Теорию, объясняющую строение и свойства тел на основе закономерностей движения и взаимодействия частиц, из которых состоят тела, называют молекулярно-кинетической.
Основные положения молекулярно-кинетической теории (МКТ) формулируются следующим образом:
· Любое вещество имеет дискретное (прерывистое) строение. Оно состоит из отдельных частиц (молекул, атомов, ионов), разделенных промежутками.
· Частицы находятся в состоянии непрерывного хаотического движения, называемого тепловым.
· Частицы взаимодействуют друг с другом. В процессе их взаимодействия возникают силы притяжения и отталкивания.
Справедливость МКТ подтверждается многочисленными наблюдениями и фактами.
Наличие у веществ проницаемости, сжимаемости и растворимости свидетельствует о том, что они не сплошные, а состоят из отдельных, разделенных промежутками частиц. С помощью современных методов исследования (электронные и ионные микроскопы) получены изображения наиболее крупных молекул.
Броуновское движение и диффузия свидетельствуют о том, что частицы находятся в непрерывном движении.
Наличие прочности и упругости тел, явления смачивания, поверхностного натяжения в жидкостях и т.д. доказывают существование сил взаимодействия между молекулами.
Масса и размеры молекул.
Размер молекул является величиной условной. Его оценивают следующим образом. Между молекулами наряду с силами притяжения действуют и силы отталкивания, поэтому молекулы могут сближаться лишь до некоторого расстояния. Расстояние предельного сближения центров молекул называют эффективным диаметром молекулы. (При этом условно считают, что молекулы имеют сферическую форму.)
С помощью многочисленных методов определения масс и размеров молекул установлено, что за исключением молекул органических веществ, содержащих очень большое число атомов, большинство молекул по порядку величины имеют диаметр 1• 10 - 10 м и массу 1• 10 - 26 кг.
Относительная молекулярная масса.
Относительной молекулярной (или атомной) массой Мr (или Аr) называют величину, равную отношению массы молекулы (или атома) mо этого вещества к 1/12 массы атома углерода mоС
Относительная молекулярная (атомная) масса является величиной, не имеющей размерности.
Количество вещества. Молярная масса. Масса молекулы.
Количеством вещества ν называют величину, равную отношению числа молекул (или атомов) N в данном теле к числу атомов NA в 0,012 кг углерода, т.е. ν = N/ NA (NA - число Авогадро).
Молярной массой М какого-либо вещества называют массу 1 моль этого вещества.
№20
Бро́уновское движе́ние — беспорядочное движение микроскопических, видимых, взвешенных в жидкости (или газе) частиц твёрдого вещества (пылинки, частички пыльцы растения и так далее), вызываемое тепловым движением частиц жидкости (или газа). Не следует смешивать понятия «броуновское движение» и «тепловое движение»: броуновское движение является следствием и свидетельством существования теплового движения.
В математике, а точнее в теории случайных процессов, броуновское движение (или винеровский процесс) — это гауссовский процесс с независимыми приращениями, у которого математическое ожидание равно нулю, а среднеквадратическое отклонение равно  .
.
№21
Все частицы твёрдых и жидких веществ расположены близко, поэтому взаимодействуют всегда, и всегда обладают потенциальной энергией. Она зависит от сил взаимодействия с «соседками» и расстояний до них.
№22
Идеальный газ — математическая модель газа, в которой предполагается, что потенциальной энергией взаимодействия молекул можно пренебречь по сравнению с их кинетической энергией. Между молекулами не действуют силы притяжения или отталкивания, соударения частиц между собой и со стенками сосуда абсолютно упруги, а время взаимодействия между молекулами пренебрежимо мало по сравнению со средним временем между столкновениями.

№23
Моле́кула (новолат. molecula, уменьшительное от лат. moles — масса[1]) — электрически нейтральная частица, состоящая из двух или более связанных ковалентными связями атомов, наименьшая частица химического вещества. В физике к молекулам причисляют также одноатомные молекулы, то есть свободные (химически не связанные) атомы (например, инертных газов, ртути и т.п.). Причисление к молекулам одноатомных молекул, то есть свободных атомов, например одноатомных газов, приводит к совместимости понятий "молекула" и "атом". Совмещение понятий "молекула" и "атом" идёт вразрез с атомно-молекулярным учением, по которому молекула образуется из атомов. Из одного атома молекула образоваться не может. Обычно подразумевается, что молекулы нейтральны (не несут электрических зарядов) и не несут неспаренных электронов (все валентности насыщены); заряженные молекулы называют ионами, молекулы с мультиплетностью, отличной от единицы (то есть с неспаренными электронами и ненасыщенными валентностями) — радикалами.Молекулы относительно высокой молекулярной массы, состоящие из повторяющихся низкомолекулярных фрагментов, называются макромолекулами.Особенности строения молекул определяют физические свойства вещества, состоящего из этих молекул.
№24
Для измерения термодинамической температуры выбирается некоторый термодинамический параметр термометрического вещества. Изменение этого параметра однозначно связывается с изменением температуры. Классическим примером термодинамического термометра может служить газовый термометр, в котором температуру определяют методом измерения давления газа в баллоне постоянного объёма. Известны также термометры абсолютные радиационные, шумовые, акустические.
Понятие абсолютной температуры было введено У. Томсоном (Кельвином), в связи с чем шкалу абсолютной температуры называют шкалой Кельвина или термодинамической температурной шкалой. Единица абсолютной температуры — кельвин (К).
Абсолютная шкала температуры называется так, потому что мера основного состояния нижнего предела температуры — абсолютный ноль, то есть наиболее низкая возможная температура, при которой в принципе невозможно извлечь из вещества тепловую энергию.
Абсолютный ноль определён как 0 K, что равно −273 °C.
№25
Теория создана немецким физиком Р. Клаузисом в 1957 году для модели реального газа, которая называется идеальный газ. Основные признаки модели:
расстояния между молекулами велики по сравнению с их размерами;
взаимодействие между молекулами на расстоянии отсутствует;
при столкновениях молекул действуют большие силы отталкивания;
время столкновения много меньше времени свободного движения между столкновениями.
№26
Средняя кинетическая энергия поступательного движения молекулы не зависит от её природы и пропорциональна абсолютной температуре газа T. Отсюда следует, что абсолютная температура является мерой средней кинетической энергии молекул.
Давление газа пропорционально произведению числа молекул в единице объема на его термодинамическую температуру.
№27
Уравнение состояния идеального газа (иногда уравнение Клапейрона или уравнение Менделеева — Клапейрона) — формула, устанавливающая зависимость между давлением, молярным объёмом и абсолютной температурой идеального газа. Уравнение имеет вид:

где
 — давление,
— давление, — молярный объём,
— молярный объём, — универсальная газовая постоянная
— универсальная газовая постоянная — абсолютная температура,К.
— абсолютная температура,К.№28
Закон Бо́йля — Марио́тта — один из основных газовых законов, открытый в 1662 году Робертом Бойлем и независимо переоткрытый Эдмом Мариоттом в 1676 году. Описывает поведение газа в изотермическом процессе. Закон является следствием уравнения Клапейрона.
Закон Бойля — Мариотта гласит:
При постоянной температуре и массе идеального газа произведение его давления и объёма постоянно.
В математической форме это утверждение записывается следующим образом

где  — давление газа;
— давление газа;  — объём газа.
— объём газа.
Важно уточнить, что в данном законе газ рассматривается, как идеальный. На самом деле, все газы в той или иной мере отличаются от идеального. Чем выше молярная масса газа, тем больше это отличие.

№29
Закон Гей-Люссака — закон пропорциональной зависимости объёма газа от абсолютной температуры при постоянном давлении, названный в честь французского физика и химика Жозефа Луи Гей-Люссака, впервые опубликовавшего его в 1802 году.
Следует отметить, что в англоязычной литературе закон Гей-Люссака обычно называют законом Шарля и наоборот. Кроме того, законом Гей-Люссака называют также химический закон объёмных отношений.
Изобарический закон, открытый Гей-Люссаком в 1802 году утверждает, что при постоянном давлении объём постоянной массы газа пропорционален абсолютной температуре. Математически закон выражается следующим образом:

или

где  — объём газа,
— объём газа, 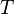 — температура.
— температура.
Если известно состояние газа при неизменном давлении и двух разных температурах, закон может быть записан в следующей форме:

или
 .
.

№30
р = рoT, где р — давление газа при абсолютной температуре Т; рo — давление газа при температуре 0оС;
a — температурный коэффициент объемного расширения газа, равный 1/273 К-1.
В том случае, когда температура выражена по шкале Цельсия, то закон Шарля имеет вид:
pt=pо (1+t),
где t — температура по шкале Цельсия, pо — давление газа при t=0° C, pt — давление газа при температуре t, — коэффициент давления, для идеальных газов a=1/273.
Закон Шарля можно сформулировать и следующим образом: для данной массы газа отношение давления газа к его температуре постоянно, если объем газа не меняется:
P/Т=const, если V=const и m=const.

№31
Газы в технике, применяются главным образом в качестве топлива; сырья для химической промышленности: химических агентов при сварке, газовой химико-термической обработке
металлов, создании инертной или специальной атмосферы, в некоторых биохимических процессах и др.; теплоносителей; рабочего тела для выполнения механической работы (огнестрельное оружие, реактивные двигатели и снаряды, газовые турбины, парогазовые установки, пневмотранспорт и др.): физической среды для газового разряда (в газоразрядных трубках и др. приборах). В технике используется свыше 30 различных Г. |
№32
Вну́тренняя эне́ргия тела (обозначается как E или U) — это сумма энергий молекулярных взаимодействий и тепловых движений молекулы. Внутренняя энергия является однозначной функцией состояния системы. Это означает, что всякий раз, когда система оказывается в данном состоянии, её внутренняя энергия принимает присущее этому состоянию значение, независимо от предыстории системы. Следовательно, изменение внутренней энергии при переходе из одного состояния в другое будет всегда равно разности между ее значениями в конечном и начальном состояниях, независимо от пути, по которому совершался переход.
Внутреннюю энергию тела нельзя измерить напрямую. Можно определить только изменение внутренней энергии:

Согласно закону Джоуля, выведенному эмпирически, внутренняя энергия идеального газа не зависит от давления или объёма. Исходя из этого факта, можно получить выражение для изменения внутренней энергии идеального газа. По определению молярной теплоёмкости при постоянном объёме,  . Так как внутренняя энергия идеального газа является функцией только от температуры, то
. Так как внутренняя энергия идеального газа является функцией только от температуры, то
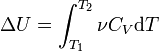 .
.
Эта же формула верна и для вычисления изменения внутренней энергии любого тела, но только в процессах при постоянном объёме (изохорных процессах); в общем случае  является функцией и температуры, и объёма.
является функцией и температуры, и объёма.
Если пренебречь изменением молярной теплоёмкости при изменении температуры, получим:
 ,
,
где  — количество вещества,
— количество вещества,  — изменение температуры.
— изменение температуры.
№33
Дата добавления: 2015-01-30; просмотров: 95 | Поможем написать вашу работу | Нарушение авторских прав |