
Проведение эксперимента значительно упрощается, если имеется возможность производить непрерывный автоматический анализ сходящего с колонки элюента. В противном случае приходится собирать элюент по фракциям или анализировать его через равные промежутки времени. Для непосредственного измерения содержания веществ в элюенте можно использовать метод определения содержания сухих веществ на рефрактометре ИРФ – 454Б2М.
Цель работы: качественное определение состава растворов
Приборы и оборудование: весы, мерные колбы объемом 100 мл, стеклянная воронка, пипетки объемом 1 и 10 мл, колонка для гель-хроматографии, мерный стакана на 500 мл, стеклянная трубка диаметром 2 – 4 мм или стеклянная палочка для отбора элюента.
Реактивы: дистиллированная вода, кристаллическая фруктоза, кристаллическая сахароза.
Ход работы:
Перед началом работы на рефрактометре необходимо проверить правильность установки шкалы показателя преломления на начальный отсчет по эталонному образцу. Рефрактометр и источник света устанавливают так, чтобы свет падал на входное окно осветительной призмы. Затем нужно откинуть осветительную призму и очистить полированное стекло измерительной призмы с помощью спирта-ректификата и резиновой груши. На очищенную таким образом поверхность осторожно, не касаясь призмы, капилляром нанести две-три капли жидкости. Опустить призму и прижать ее специальным крючком. Измерения проводят в проходящем свете. Жидкость должна равномерно распределиться по всей поверхности, но не выступать по краям.
 Поворотом кольца устранить окрашенность границы светотени. Добиться наиболее качественного изображения границы светотени изменением положения рефрактометра относительно источника света. Затем установить на соответствующей шкале табличный показатель преломления эталонной жидкости (дистиллированная вода – 1,3333).
Поворотом кольца устранить окрашенность границы светотени. Добиться наиболее качественного изображения границы светотени изменением положения рефрактометра относительно источника света. Затем установить на соответствующей шкале табличный показатель преломления эталонной жидкости (дистиллированная вода – 1,3333).
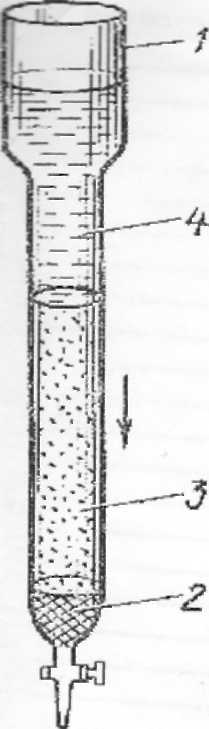
| Рисунок 4. Хроматографическая колонка. 1 – стеклянная трубка, 2 – тампон стеклянной ваты, 3 – сорбент, 4 – анализируемый раствор |
Для подготовки хроматографической колонки в мерный цилиндр вместимостью 500 см3 помещают 5 г сухого сефадекса G-25, заливают водой до метки и оставляют для набухания на сутки. Затем содержимое цилиндра перемешивают до получения однородной системы. Перед заполнением колонки воздух из набухшего сефадекса удаляют перемешиванием. В нижнюю узкую часть колонки помещают тампон из стекловаты, служащий опорой для носителя. После заполнения колонки гелем на требуемую высоту (25 см) продолжают пропускать воду, оставшеюся в колонке, так чтобы над поверхностью сефадекса образовался слой жидкости высотой 1 см, не допускать проскока жидкости ниже уровня сефадекса.
Перед проведением анализа готовят растворы анализируемых веществ, для этого на весах взвешивают 1,5 г фруктозы и 1,5 г сахарозы, после чего их помещают в мерную колбу на 100 мл и добавляют дистиллированной воды до метки.
Перед внесением раствора в колонку опускают уровень жидкости до уровня геля. Необходимо следить, чтобы верхний слой геля не пересыхал. После этого осторожно пипеткой вносят анализируемый раствор объемом 1 мл. Когда раствор впитается полностью в гель, осторожно в один прием, по стенке вводят в верхнюю часть колонки промывной жидкости (дистиллированную воду), стараясь не взмутить верхний слой сефадекса. Одновременно под край колонки помещают мерный цилиндр вместимостью 25 см и открывают кран. Для определения берут каждую пятую каплю элюента и определяют показатель преломления на рефрактометре. Анализ продолжают до тех пор, пока показатель преломления возрастёт, а затем понизится до первоначального значения. При отборе элюента для анализа измеряют объем жидкости в мерном цилиндре. Очень важно установить объем Рисунок 5. Форма для построения графика зависимости концентраций элюента от вышедшего объема промывной жидкости
элюента, при котором концентрация веществ будет максимальной.
После определения строят графики зависимости концентраций элюента от вышедшего объема промывной жидкости.
Пример: Определение молекулярной массы инулина в инулиносодержащем концентрате
Таблица 8. Параметры частной калибровки
| Стандарт | Молекулярная масса, Да | Логарифм молекулярной массы | Удерживаемый объем,см3 |
| ПЭГ-6000 | 6000,00 | 3,78 | 27,5 |
| ПЭГ-3000 | 3000,00 | 3,48 | 34,2 |
| ПЭГ-2000 | 2000,00 | 3,30 | 36,2 |
| ПЭГ-100 | 100,00 | 2,00 | 56,2 |
| Сахароза | 342,30 | 2,53 | 45,5 |
| Глюкоза | 180,16 | 2,26 | 51,0 |
| Фруктоза | 180,17 | 2,25 | 52,3 |
| Биодобавка из топинамбура | Х | Х | 30,0 |

Рисунок 6. Хроматограмма веществ при элюировании через колонку

Рисунок 7. Зависимость между удерживаемыми объемами и относительными молекулярными массами исследуемых веществ Lgх = 3,71 Молекулярная масса: ~ 5200 Да
Дата добавления: 2015-09-11; просмотров: 75 | Поможем написать вашу работу | Нарушение авторских прав |