
Читайте также:
|
Анализ водной вытяжки из почвы дает сведения о составе и количестве легкорастворимых веществ почвы и позволяет установить степень и характер засоления почвы.
Состав водной вытяжки из почв
При действии воды на почву происходит растворение минеральных соединений и частично гумусовых веществ, а в некоторых случаях идет также процесс разложения сложных силикатов. В дальнейшем почва взаимодействует уже не с водой, а с образовавшимся сложным раствором, где могут протекать реакции взаимного обмена между катионами вытяжки и катионами поглощающего комплекса почвы. Щелочная реакция почв увеличивает растворимость гумусовых веществ, кислая реакция почв повышает растворимость полуторных оксидов. В связи с этим условия и время приготовления водной вытяжки должны быть строго стандартными. Общепринято приготовлять водную вытяжку из почвы (измельченная и просеянная средняя проба) путем пятиминутного взбалтывания ее с водой, не содержащей СО2, при соотношении почвы к воде 1:5.
Важной характеристикой свойств почвы является величина рН водной суспензии. В зависимости от значения рН определяют кислотность или щелочность водной вытяжки почвы и выбирают соответствующий ход дальнейшего анализа. В водной вытяжке из почвы чаще всего определяют анионы: СO32-, HCO3-, Cl-, SO42- и катионы: Ca2+, Mg2+, K+, Na+. В специальных случаях проводят определение HSiO3-, H2PO4-, HPO42-, Fe3+, Fe2+, Al3+, NH4+ и др., общей минерализации, общей щелочности, общей кислотности, водно-растворимых органических веществ (окисляемости) и т.д.
Результаты анализа принято выражать количеством мг-экв вещества на 100 г почвы.
Определение рН
Определение величины рН проводят в фильтрате сразу после приготовления водной вытяжки из почвы или, что более правильно, в суспензии (до фильтрования). Для измерения рН суспензию готовят при отношении почвы к воде 1:2,5 (20 г почвы и 50 мл дистиллированной воды). Определение рН проводят с помощью рН-метра.
Приготовление водной вытяжки из почв
Состав водной вытяжки меняется при соприкосновении ее с почвой и с воздухом, поэтому все определения проводятся в возможно короткий срок. Прежде чем приступить к приготовлению водной вытяжки, следует собрать установку для фильтрования и приготовить необходимые для дальнейших определений реагенты.
На технических весах отвешивают 100 г воздушно-сухой почвы (средняя проба) и количественно переносят в емкость для взбалтывания. Отмеряют мерной колбой 500 мл дистиллированной воды, не содержащей СО2. Получают гетерогенную систему, в которой отношение почвы к воде равно 1:5. Емкость закрывают пробкой и энергично встряхивают 5 мин. По окончании взбалтывания всю суспензию почвы с водой, не давая ей отстояться, осторожно и быстро фильтруют. Фильтр помещают в воронку диаметром 15 – 20 см. Одиночный фильтр легко прорывается при перенесении на него почвы, поэтому под него подкладывают беззольный фильтр. Нельзя допускать, чтобы фильтр был выше воронки; в этом случае раствор, поднимаясь по капиллярам бумаги, образует "выцветы" солей по краю фильтра и тем самым снижает концентрацию их в фильтрате. Фильтрование следует проводить в комнате, свободной от паров HCl и других кислот, а также от паров аммиака. В качестве приемника используют сухую коническую колбу на 500 мл. Если первые порции фильтрата окажутся мутными, то его следует перефильтровать через этот же фильтр сразу, не дожидаясь конца фильтрования. По окончании фильтрования колбу с фильтратом следует закрыть сухой пробкой.
Все количественные определения из водной вытяжки необходимо проводить сразу после ее приготовления.
Таблица
Множители пересчета объема вытяжки на 100 г почвы (при соотношении почвы к воде или другому растворителю как 1:5)
| Анализируемый объем, мл | Вес почвы, соответствующий анализируемому объему, г | Множитель пересчета на 100 г почвы |
| 0,2 | 2,5 |
Определение общей и частной щелочности (карбонатов и гидрокарбонатов)
Щелочность водной вытяжки из почвы обусловлена присутствием в ней растворимых карбонатов и гидрокарбонатов. Суммарное содержание ионов СО32- и НСО3- соответствует общей щелочности, содержание СО32- – частной щелочности.
Определение карбонатов и гидрокарбонатов при совместном присутствии аналогично титрованию двух слабых оснований, одно из которых является двухкислотным:
СО32- + Н+ ↔ НСО3-
НСО3- + Н+ ↔ Н2СО3
Если вести титрование такой смеси с использованием двух индикаторов – фенолфталеина и метилового оранжевого, то по фенолфталеину двухкислотное основание (СО32-) будет оттитровано по первой стадии; при дальнейшем титровании по метиловому оранжевому будет оттитровано второе основание (НСО3-) и первое основание (СО32- перешедший в НСО3-) до конца.
Методика определения. Аликвоту водной вытяжки (25 мл) переносят в колбу для титрования, добавляют 2 капли фенолфталеина и осторожно, по каплям титруют 0,01 н. раствором HCl до исчезновения розовой окраски (V1). В обесцветившийся раствор добавляют 2 капли метилового оранжевого и дотитровывают по каплям 0,01 н. раствором HCl до перехода окраски из желтой в оранжевую. Если рН водной вытяжки почвы менее 8, то определяют щелочность только с индикатором метиловым оранжевым.
Результаты определения выражают количеством мг-экв СО32- (m1) и НСО3- (m2) на 100 г почвы:


где р – навеска почвы в объеме 25 мл водной вытяжки (см. табл.1).
Тогда частная щелочность соответствует m1, а общая щелочность –

Определение кальция и магния (жесткости)
Определение кальция и магния проводят с помощью комплексонометрического титрования. В одной порции раствора определяют суммарное содержание кальция и магния, титруя раствором ЭДТА в присутствии индикатора ЭХЧТ в условиях аммиачного буфера; в другой порции раствора определяют кальций, проводя титрование в сильнощелочной среде в присутствии индикатора мурексид. Содержание магния находят по разности.
Методика определения. Аликвоту водной вытяжки 10 мл переносят в колбу для титрования и добавляют 50 мл воды. Добавляют 5 мл 2н. раствора NaOH, мурексид на кончике шпателя и титруют 0,025 М раствором ЭДТА до перехода окраски из розовой в лиловую (V1).
Следующую аликвоту водной вытяжки 10 мл переносят в колбу для титрования, добавляют 50 мл воды, 5 мл аммиачного буферного раствора. Вносят индикатор ЭХЧТ на кончике шпателя и титруют 0,025 М раствором ЭДТА до перехода окраски из сиреневой в синюю (V2).
Результаты анализа выражают количеством мг-экв Са2+ и Mg2+ на 100 г почвы:


Определение нитрит-ионов
Нитрит-ионы являются промежуточным продуктом биохимического окисления аммиака или восстановление нитрат-ионов. Для их определения предлагается фотометрический метод с сульфаниловой кислотой и a-нафтиламином. Метод основан на диазотировании сульфаниловой кислоты присутствующими в пробе нитритам-ионами и реакции полученной соли с a-нафтиламином с образованием красно-фиолетового азокрасителя. Интенсивность окраски пропорциональна концентрации нитрит-ионов.
Методика определения. Для определения берут аликвоту водной вытяжки 2 мл в колбу на 50 мл, прибавляют 1 мл раствора сульфаниловой кислоты и смесь тщательно перемешивают. После пятиминутного стояния прибавляют 1 мл раствора a-нафтиламина, разбавляют водой до метки, перемешивают. Через 40 минут замеряют оптическую плотность раствора при длине волны 540 нм в кювете толщиной 5 см на фоне дистиллированной воды.
Результаты анализа выражают количеством мг-экв нитрит-ионов на 100 г почвы
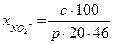
где с – содержание нитрит-ионов, найденное по ГГ, мг/л; р – навеска почвы в объеме 2 мл водной вытяжки (см. табл.1); 46 – эквивалент нитрит-иона; 20 – разбавление (1000 мл /50 мл).
Определение водно-растворимых органических веществ (общей окисляемости)
Почвенные воды и водные вытяжки из почв содержат водно-растворимые органические вещества, количество которых характеризует "подвижность" гумуса. О количестве органических веществ судят по количеству окислителя, необходимому для их окисления, т.е. по "окисляемости" таких растворов. В зависимости от используемого окислителя различают "перманганатную" и "бихроматную" окисляемость (они не одинаковы). Оба вида окисляемости определяются косвенными методами – титрованием избытка окислителя, не вошедшего в реакцию с органическими веществами.
Определение перманганатной окисляемости
Органические вещества окисляются в кислой среде перманганатом калия при нагревании, избыток его разрушается оксалатом натрия или щавелевой кислотой, а избыток последних оттитровывают перманганатом калия, т.к. непосредственно избыток перманганата калия оттитровать оксалатом натрия затруднительно вследствие выделения значительного выделения MnO2. Метод можно использовать только для проб, окисляемость которых ниже 100 мг О/ л.
Методика определения. В колбу для титрования помещают несколько стеклянных шариков или кусочков керамики и вносят 10 мл аликвоты, доводят водой до 100 мл, приливают 5 мл разбавленной H2SO4 и 20 мл 0,01 н. раствора KMnO4. Смесь нагревают так, чтобы она закипела через 5 мин и кипятят 10 мин. К горячему раствору прибавляют 20 мл 0,01 н. раствора Н2С2О4. Обесцвеченную смесь титруют горячей (лучше при 80-90°С) 0,01 н. раствором KMnO4 до розового окрашивания.
Если раствор при кипячении обесцветится или побуреет, то определение повторяют с разбавленной пробой.
Результаты анализа выражают количеством мг-экв окисляющих веществ в 1 л раствора

где V1 и V2 – объемы KMnO4, пошедшие на окисление органических веществ и щавелевой кислоты, V3 – объем щавелевой кислоты, V4 – объем анализируемой пробы, мл.
Также можно результаты определения водорастворимых органических соединений вычислять в процентном содержании углерода или перегноя:

где М – множитель для пересчета взятого объема вытяжки на 100 г почвы, 0,003 – граммовое значение мг-экв углерода.
Определение фосфат-ионов
Доступный для питания растений фосфор находится в почве преимущественно в виде соединений с кальцием, магнием и полуторными оксидами. Во все методах определения усвояемого, или доступного, фосфора количественный учет Р2О5 ведут фотометрическим методом. Метод основан на частичном восстановлении Мо (VI) фосфорномолибденовой гетерополикислоты до низших валентностей, в результате чего образуется молибденовая синь, интенсивность окраски которой пропорциональна концентрации фосфат-ионов в растворе.
Приготовление составного реактива. К 300 мл бидистиллята приливают при перемешивании 144 мл концентрированной серной кислоты H2SO4. Затем охлаждают приблизительно до 20°С и при перемешивании добавляют раствор 10 г сульфаминовой кислоты NH2SO3H в 100 мл дистиллированной воды, раствор 12,5 г молибдата аммония (NH4)2MoO4·4H2O в 200 мл дистиллированной воды, раствор 0,235 г хлорида сурьмы SbCl3 и 0,6 г винной кислоты или 0,345 г антимонилтартрата калия KSbOC4H4·0,5H2O в 100 мл дистиллированной воды. После этого разбавляют смесь до 1 л дистиллированной водой. Реактив хранят в склянке из оранжевого стекла.
Методика определения. Берут аликвоту 5 мл водной вытяжки в мерную колбу на 50 мл, добавляют 2 мл составного реактива, перемешивают. Затем добавляют 0,5 мл аскорбиновой кислоты, разбавляют водой до метки и перемешивают. Оптическую плотность замеряют через 15-20 мин при длине волны 670 нм в кювете с толщиной 5 см на фоне дистиллированной воды.
Результаты анализа выражают количеством мг-экв фосфат-ионов на 100 г почвы

где с – содержание фосфат-ионов, найденное по ГГ, мг/л; р – навеска почвы в объеме 5 мл водной вытяжки (см. табл.1); 95 – эквивалент фосфат-иона; 20 – разбавление (1000 мл /50 мл).
Результаты анализа можно также выразить в виде мг-экв оксида фосфора на 100 г почвы

где 142/95×2 – фактор пересчета фосфат-иона на оксид фосфора.
Определение фторид-ионов в почве
Пробоподготовка. Для определения содержания водорастворимой формы фтора точную навеску тонкоизмельченной пробы 5 г помещают в полиэтиленовую емкость, добавляют 50 мл воды. Содержимое встряхивают в течение 15 мин и оставляют на ночь. После стояния содержимое перемешивают круговыми движениями и фильтруют.
Приготовление составного реактива. В мерной колбе на 250 мл растворяют 0,0526 г безводного ализаринкомплексона в 30 мл воды с добавлением нескольких капель концентрированного аммиака, добавляют 100 мл диметилформамида (ДМФА) и 37,5 мл ацетатного буферного раствора (рН 4,1 – 4,2). После тщательного перемешивания добавляют 2,5 мл 0,05 М раствора нитрата лантана, доводят водой до метки и перемешивают (раствор можно хранить в течение 6 месяцев).
Построение градуировочного графика. Для построение градуировочного графика в мерные колбы на 25 мл вводят 0,5; 1; 1,5; 2; 2,5 мл раствора фторида натрия с титром по фтору 19 мкг/мл, добавляют 10 мл составного реактива АК-La и доводят водой до метки. Полученные растворы тщательно перемешивают и через 20 мин замеряют оптическую плотность при длине волны 620 нм. Измерения проводят в кювете с толщиной 1 см на фоне составного реактива той же концентрации.
Определение концентрации фторид-ионов. Из фильтрата отбирают аликвоту 10 мл в мерную колбу на 25 мл, добавляют 10 мл составного реактива и доводят водой до метки. Перемешивают и замеряют оптическую плотность как при построении ГГ.

Результаты анализа выражают количеством мг-экв фтора на 100 г почвы

где с – содержание фторид-ионов, найденное по ГГ, мкг/25 мл раствора; р – навеска почвы в объеме 10 мл водной вытяжки (см. табл.1); 19 – эквивалент фосфат-иона.
Дата добавления: 2015-04-12; просмотров: 126 | Поможем написать вашу работу | Нарушение авторских прав |