
Читайте также:
|
Реакции в растворах электролитов, при которых не изменяется заряд ионов, входящих в соединения, называются ионообменными. Например, взаимодействие электролитов в состоянии равновесия
К1А1 + К2А2 D К1А2 + К2А1.
Константа равновесия
 (4)
(4)
Чтобы узнать, в какую сторону смещено данное равновесие, рассмотрим диссоциацию каждого из 4-х электролитов:
К1А1⇆К1⁺ + А 1 -  ;
;
К2А2⇆К2⁺ + А2⁻ 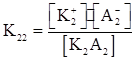 ;
;
К1А2⇆К1⁺+А2⁻  ;
;
К₂А₁⇆К₂⁺+А₁⁻  .
.
Подставляя в уравнение (4) вместо концентраций значения К, получим
 .
.
Если К>1, т.е. К₁₁· К₂₂>К₁₂·К₂₁, то равновесие смещено вправо (легче идёт прямая реакция).
Если К<1,т.е. К₁₁·К₂₂<К₁₂·К₂₁, то равновесие смещено влево (в сторону обратной реакции).
При К→ ∞ реакция будет необратимой.
Равновесие в ионообменных реакциях смещается в сторону образования наименее диссоциированных соединений.
Ионообменные реакции протекают в растворах электролитов в следующих случаях:
1) если образуется осадок трудно растворимого вещества;
2) если образуется газ (легколетучее вещество);
3) если образуется слабый электролит (плохо диссоциирующее соединение);
4) если образуется комплексный ион.
В уравнениях ионных реакции формулы сильных электролитов записывают в диссоциированном виде, слабых – в недиссоциированном.
Примеры:
1.Образование осадков:
AgNO3 + NaCl = AgCl↓ + NaNO3;
Ag+ + NO₃¯ + Na+ + CI¯ = AgCl + Na+ + NO₃¯;
Ag+ + Cl¯ = AgCl.
2. Образование газов:
Na₂S + H₂SO₄ = Na2SO4 + H2S↑;
2 Na+ + S²¯+ 2 H+ + SO₄²¯ = H2S↑ + 2 Na+ + SO₄²¯;
2 H+ + S²¯= H₂S↑.
3. Образование слабых электролитов. Чаще всего это – образование воды,
слабого основания или слабой кислоты:
а) образование воды:
NaOH + HCl = H₂O + NaCl;
Na+ + OH⁻ + H+ + Cl⁻ = H₂O + Na+ + Cl⁻;
H+ + OH⁻ = H₂O;
б) образование слабого основания:
NH₄Cl + KOH = NH₄OH + KCl;
NH₄+ + Cl⁻ + K+ + OH⁻= NH₄OH + K++ Cl⁻;
NH₄+ + OH⁻ = NH₄ОН;
в) образование слабой кислоты:
2 CH₃COONa + H₂SO₄ = 2 CH₃COOH + Na₂SO₄;
2 CH₃COO⁻ + 2 Na+ + 2 H+ + SO₄²⁻ = 2 CH₃COOH + 2 Na+ + SO₄²⁻;
CH₃COO⁻ + H+ = CH₃COOH.
4. Образование комплексного иона (например, катиона)
CuSO₄ ∙ 4 H₂O + 4 NH₃ = [Cu(NH₃)₄]SO₄ + 4 H₂O;
[Cu(H₂O)₄]²+ + SO₄²⁻ + 4 NH₃ = [Cu(NH₃)₄]²+ + SO₄²⁻ + 4 H₂O.
Дата добавления: 2015-09-10; просмотров: 147 | Поможем написать вашу работу | Нарушение авторских прав |