
Читайте также:
|
1. Кислотные свойства.
Фенолы являются кислотами более сильными, чем спирты и вода, но слабее угольной кислоты. Поэтому фенолы легко реагируют с раствором едкого натра с образованием фенолята:

Электронодонорные заместители в пара- орто-положениях понижают кислотные свойства. Электроноакцепторные заместители в пара- и орто-положениях повышают кислотные свойства. Так 2,4,6-тринитрофенол обладает выраженными кислотными свойствами. Поэтому называется пикриновой кислотой. Способен вытеснять угольную кислоту из ее солей, т.е. способен образовывать фенолят в растворе соды.
Связь между углеродом бензольного кольца и атомом кислорода гидроксильной группы обладает повышенной прочностью за счет частичной двоесвязанности. Поэтому реакции с разрывом связи С-О для фенола не характерны.
Восстановление
К числу реакций, протекающих с разрывом связи С-О, относится восстановление фенола цинковой пылью при перегонке. В ходе реакции гидроксильная группа замещается водородом:

Другим примером разрыва связи С-О является нуклеофильное замещение гидроксильной группы в активированных фенолах. Например, замещение гидроксильной группы в 2,4,6-тринитрофеноле на галоид по механизму «присоединение-отщепление»:

В основном химические свойства фенола формируют реакции, протекающие с разрывом связи С-Н, а также реакции замещения ароматическое кольцо.
О-алкилирование
Сам фенол является слабым основанием, поэтому в реакции алкилирования с галоидными алкилами обычно используют фенолят натрия:

О-ацилирование
Кислотные свойства фенола играют позитивную роль в реакциях фенола с хлорангидридами и ангидридами карбоновых кислот:
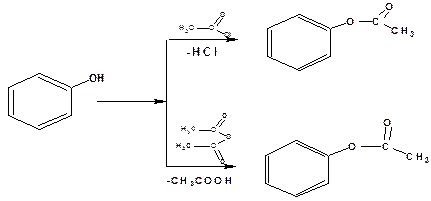
В форме фенолята фенол ацилируется хлорангидридом бензойной кислоты, поскольку у хлорангидрида бензойной кислоты связь хлора и углерода более прочная, чем такая связь в хлорангидридах алифатических кислот:
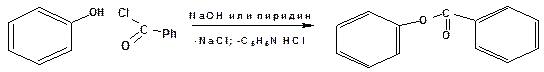
С хлорангидридами минеральных кислот также образуются эфиры. Причем с пятихлористым фосфором образуются эфиры, хлорированные в ароматическое кольцо.
Реакции замещения
Галогены реагируют с фенолом без катализатора. Фенол взаимодействует с бромом в водном растворе. Причем реакция не останавливается на стадии монобромирования. В начале образуется 2,4,6-трибромфенол, а затем тетрабромпроизводное:

Аналогично под действием концентрированной азотной кислоты в присуствии серной кислоты фенол превращается в тринитрофенол (пикриновую кислоту):

Мононитрофенолы образуются при нитровании фенола разбавленной азотной кислотой в среде уксусной кислоты при комнатной температуре:

Два полученные изомера существенно различаются по своим свойствам. орто -нитрофенол, в отличие от пара-изомера, не растворяется в воде, имеет более низкую температуру кипения и перегоняется с водяным паром. Эти особенные свойства орто- нитрофенола обусловлены наличием внутримолекулярной водородной связи:

Ориентация электрофильного замещения в орто-положение характерно для фенола. Так сульфирование фенола при температуре 15-200С приводит к образованию орто -фенолсульфокислоты, а при температуре 1000С образуется пара -фенолсульфокислота:

Различие условий указывает, что орто -фенолсульфокислота явяляется продуктом кинетически контролируемым, а образование пара -фенолсульфокислоты контролируется термодинамически.
Реакция Реймера-Тимана:
При взаимодействии фенола со щелочным раствором хлороформа образуется салициловый альдегид:

Реакция Кольбе-Шмитта
При взаимодействии сухого фенолята натрия с углекислым газом образуется салициловая кислота:

Реакция с формальдегидом
Фенолы легко конденсируются с формальдегидом (а также уксусным альдегидом, бензальдегидом, фталевым ангидридом, ацетоном) в присутствии кислот или щелочей. Конденсация с формальдегидом проходит по следующему механизму:
 При низкой температуре образуется полимер линейного строения, замещение только в орто-положение. При высокой температуре образуются продукты пара-замещения что приводит к пространственной сшивке полимера. Таким образом, получают фненолформальдегидные смолы.
При низкой температуре образуется полимер линейного строения, замещение только в орто-положение. При высокой температуре образуются продукты пара-замещения что приводит к пространственной сшивке полимера. Таким образом, получают фненолформальдегидные смолы.
Окисление
При окислении фенола пероксидом водорода в присутствии железного катализатора образуется пирокатехин:

При действии хромовой кислоты на фенол и гидрохинон образуется п -бензохинон, из пирокатехина получается о -бензохинон:

Восстановление
Пр гидрировании водородом в присутствии катализатора фенолы превращаются в спирты, производные циклогексана:

Дата добавления: 2015-09-11; просмотров: 86 | Поможем написать вашу работу | Нарушение авторских прав |