
Читайте также:
|
К кинетически сложным реакциям относятся: обратимая реакция, например, реакция первого порядка k₁
A B
k₁
k₁ В
параллельные реакции, например, реакции типа А
k₂ С
k₁k₂
и последовательные реакции типа А В С
Кинетика приведенной выше обратимой реакции описывается уравнением:
k₁ + k₂ =  ln
ln 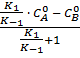 (88)
(88)
Кинетика приведенных параллельных реакций описывается уравнением:
k₁ + k₂ =  ln
ln  (89)
(89)
где х – количество вещества, вступившее в реакцию к моменту времени от начала опыта, моль.
Кинетика последовательных превращений с промежуточным соединением В, рассмотренных выше, описывается уравнением:
СА = 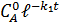 ;CB =
;CB = 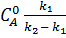 (
(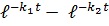 ) (90)
) (90)
CC = 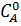 (1 ―
(1 ―  ∙
∙ 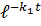 +
+ 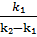 ∙
∙ 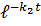 ).
).
Максимальная концентрация промежуточного соединения Вв схеме последовательных превращений достигается за время: t = ln 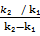 (91)
(91)
Дата добавления: 2015-02-22; просмотров: 128 | Поможем написать вашу работу | Нарушение авторских прав |